
 H++CN-,用①-②可得HCN电离的热化学方程式为:
H++CN-,用①-②可得HCN电离的热化学方程式为: H+(aq)+CN-(aq)△H=-12.1kJ?mol-1-(-55.6kJ?mol-1)=+43.5kJ?mol-1,
H+(aq)+CN-(aq)△H=-12.1kJ?mol-1-(-55.6kJ?mol-1)=+43.5kJ?mol-1,

科目:高中化学 来源: 题型:
| 弱酸 | CH3COOH | H2SO3 | HCN |
| 物质的量浓度mol/L | 0.01 | 0.01 | 0.01 |
| pH | 3.4 | 2.3 | 5.6 |
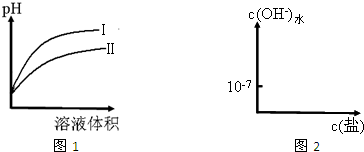
 HSO3-+OH-
HSO3-+OH- HSO3-+OH-
HSO3-+OH-| c(H+) |
| c(CH3COOH) |
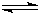 H+(aq)+CN-(aq)△H=+43.5kJ?mol-1
H+(aq)+CN-(aq)△H=+43.5kJ?mol-1 HCN(aq)+OH-(aq)的△H=
HCN(aq)+OH-(aq)的△H=查看答案和解析>>
科目:高中化学 来源:2013届河北省高二上学期期中考试化学试卷(解析版) 题型:选择题
已知:HCN(aq)与NaOH(aq)反应的 ;HCl(aq)与NaOH反应的
;HCl(aq)与NaOH反应的 ,则HCN在水溶液中电离的
,则HCN在水溶液中电离的 等于
等于
A.
 B.- 43.5
B.- 43.5 C.+ 43.5
C.+ 43.5 D.+ 67.7
D.+ 67.7
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 弱酸 | CH3COOH | H2SO3 | HCN |
| 物质的量浓度mol/L | 0.01 | 0.01 | 0.01 |
| pH | 3.4 | 2.3 | 5.6 |
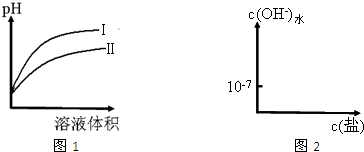
| c(H+) |
| c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源:2011年浙江省宁波市余姚中学高考化学二模试卷(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com