
| A. | 0.4 mol/L | B. | 0.2mol/L | C. | 0.1mol/L | D. | 0.05mol/L |
分析 n(HCl)=0.1L×0.6mol/L=0.06mol,n(OH-)=0.1L×0.4mol/L×2=0.08mol,则混合后碱过量,结合c=$\frac{n}{V}$计算.
解答 解:n(HCl)=0.1L×0.6mol/L=0.06mol,n(OH-)=0.1L×0.4mol/L×2=0.08mol,则混合后碱过量,
剩余的OH-物质的量为0.08mol-0.06mol=0.02mol,
反应后溶液体积为200mL,则混合溶液中OH-物质的量浓度为$\frac{0.02mol}{0.2L}$=0.1mol/L,
故选C.
点评 本题考查物质的量浓度的计算,为高频考点,把握酸碱中和的实质及物质的量关系为解答的关键,侧重分析与计算能力的考查,注意混合时过量判断,题目难度不大.


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钡溶液与稀硫酸的反应:OH-+H++Ba2++SO42-=BaSO4↓+H2O | |
| B. | 硫酸铝溶液中加入过量氨水:Al3++4OH-═[Al(OH)4]- | |
| C. | 用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+=Cu2++2Fe2+ | |
| D. | 碳酸钙溶于稀盐酸中:CO32-+2H+=H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(H+)=c(CH3COO-)+c(OH-) | B. | c (Na+)>c (CH3COO-)>c(OH-)>c(H+) | ||
| C. | c(Na+)=c(CH3COO-)>c(OH-)=c(H+) | D. | c (CH3COO-)>c(Na+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba2+ K+ OH- NO3- | B. | Na+ Ca2+ HCO3- NO3- | ||
| C. | Ag+ K+ Cl- NO3- | D. | Na+ Cu2+ SO42- Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子晶体中一定存在共价键和范德华力 | |
| B. | 由非金属元素组成的化合物一定是共价化合物 | |
| C. | 原子晶体和分子晶体一定均含有共价键,离子晶体也可能含有共价键 | |
| D. | 两个非金属元素原子间不可能形成离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤的气化就是将煤在高温条件由固态转化为气态的物理变化过程 | |
| B. | 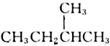 和 和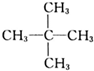 互为同分异构体 互为同分异构体 | |
| C. | 淀粉、蛋白质和油脂都是高聚物,在一定条件下都能水解 | |
| D. | 石油裂解可以得到更多的汽油,这种汽油是一种纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
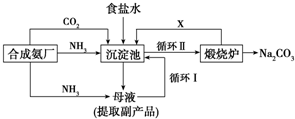
| 实验方案 | 预测现象 | 预测依据 |
| 操作1:向2mL Na2CO3溶液中滴加1mL 0.5mol•L-1 CaCl2溶液 | 有白色沉淀 | Na2CO3溶液中的CO32-浓度较大,能与CaCl2发生反应:Ca2++CO32-═CaCO3↓ (离子方程式) |
| 操作2:向2mL NaHCO3溶液中滴加1mL 0.5mol•L-1CaCl2溶液 | 无白色沉淀 | NaHCO3溶液中的CO32-浓度很小,不能与CaCl2反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com