
下列关于反应热的说法正确的是()
A. 当△H为“﹣”时,表示该反应为吸热反应
B. 已知C(s)+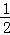 O2(g)=CO(g)的反应热为110.5kJ/mol,说明碳的燃烧热为110.5kJ
O2(g)=CO(g)的反应热为110.5kJ/mol,说明碳的燃烧热为110.5kJ
C. 反应热的大小与反应物所具有的能量和生成物所具有的能量无关
D. 化学反应的反应热只与反应体系的始态和终点状态有关,而与反应的途径无关
考点: 反应热和焓变.
专题: 化学反应中的能量变化.
分析: A、△H<0时,反应为放热反应;
B、根据燃烧热的含义来判断;
C、反应热取决于反应物和生成物的能量大小关系;
D、根据盖斯定律知识来回答.
解答: 解:A、△H<0的反应为放热反应,即当△H为“﹣”时,表示该反应为放热反应,故A错误;
B、燃烧热的含义:完全燃烧1mol物质生成最稳定的氧化物所放出的能量,碳的燃烧热应该是生成二氧化碳时所放出的能量,故B错误;
C、反应热取决于反应物和生成物的能量大小关系,当反应物能量大于生成物能量,反应为放热反应,反之则为吸热反应,故C错误;
D、根据盖斯定律可知化学反应的反应热只与反应体系的始态和终点状态有关,而与反应的途径无关,故D正确.
故选D.
点评: 本题考查反应热,注意反应热和焓变知识是热化学部分的重点,学生可以根据所学知识解答,注意平时知识的积累是关键.


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
9.75g锌与0.3 mol的盐酸刚好完全反应,放出0.15 mol H2,在溶液中有0.15mol Zn2+离子和0.3 mol Cl﹣离子,把反应后的溶液蒸干,可以得到ZnCl20.15 mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
沼气是一种能源,它的主要成分是CH4,0.5molCH4完全燃烧生成CO2和液态水时放出445kJ的热最,则下列热化学方程式中正确的是()
A. 2CH4(g)+4O2(g)=2CO2(g)+4H2O(g)△H=+890kJ•mol﹣1
B. CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=+890kJ•mol﹣1
C. CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=﹣890kJ•mol﹣1
D. 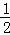 CH4(g)+O2(g)=CO2(g)+H2O(l)△H=﹣890kJ•mol﹣1
CH4(g)+O2(g)=CO2(g)+H2O(l)△H=﹣890kJ•mol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醛在酸性催化剂存在下三分子聚合可以生成性质相对稳定、毒性小、易于运输的三聚甲醛,反应如图所示.下列说法正确的是()

A. 甲醛水溶液可作为食物防腐剂
B. 该反应类型为缩聚反应
C. 三聚甲醛分子中既含σ键又含п键
D. 常温下,9g三聚甲醛中含1.806×1023个碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
已知前四周期五种元素X、Y、Z、W、T,它们的原子序数依次增大.X是空气中含量最多的元素;Y、W位于同周期,W单质在常温下是黄绿色气体,Y单质在其中燃烧发出黄色火焰;Z的氧化物常用作制备通讯光纤;T是常见金属,在氧气中燃烧可以得到具有磁性的黑色物质.回答下列问题:
(1)Z位于元素周期表中第三周期第ⅣA族;W基态原子核外电子排布式为 .
(2)Y和W的简单离子比较,半径较大的是 (填离子符号);键的极性比较:X﹣H Z﹣H(填“大于”或“小于”);Z单质和其氧化物比较,熔点较高的是 (填化学式).
(3)向T单质与稀硫酸反应后的溶液中滴加足量的NaOH溶液,能观察到的现象是 ;X与Y形成的原子个数比为1:3的简单化合物可与水反应生成两种碱,写出该物质与醋酸溶液反应的化学方程式 .
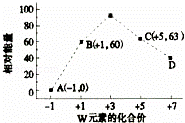
(4)一定条件下,在水溶液中1molW﹣、WO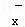 (z=1,2,3,4等)的能量(kJ)相对大小如图所示.
(z=1,2,3,4等)的能量(kJ)相对大小如图所示.
①D点对应的微粒是ClO4﹣(填离子符号).
②写出B→A+C反应的热化学方程式: (用离子符号表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
2HI(g)⇌H2(g)+I2(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是()
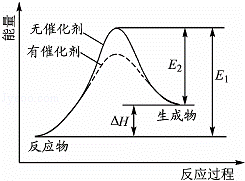
A. 升高温度,反应速率增大,△H减小
B. 升高温度,不影响活化分子百分数
C. 催化剂能降低该反应的活化能
D. 逆反应的活化能等于正反应的活化能
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙两个容器内都进行A→B的反应,甲容器内每分钟减少了4mol A,乙容器内每分钟减少2mol A,则甲容器内的反应速率比乙容器内的反应速率()
A. 快 B. 慢 C. 相等 D. 无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
能源危机是当前全球问题,开源节流是应对能源危机的重要举措.
(1)下列做法有助于能源“开源节流”的是 (填字母).
a.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
b.大力开采煤、石油和天然气以满足人们日益增长的能源需求
c.开发太阳能、水能、风能、地热等新能源,减少使用煤、石油等化石燃料
d.减少资源消耗,增加资源的重复使用、资源的循环再生
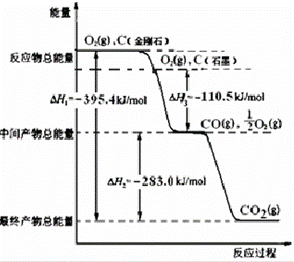
(2)金刚石和石墨均为碳的同素异形体,氧气不足时它们燃烧生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如图所示:
(a)通常状况下,金刚石和石墨中 (填“金刚石”或“石墨”)更稳定,石墨的燃烧热为△H= kJ•mol﹣1.
(b)12g石墨在一定量空气中燃烧,生成气体36g,则该过程共放出的热量 kJ.
(3)已知:N2(g)+O2(g)=2NO(g);△H=+180.0kJ•mol﹣1.综合上述有关信息,请写出用CO除去NO的热化学反应方程式
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法或表示正确的是()
A. 等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B. 物质发生化学变化时一定伴随着吸热现象或放热现象
C. 稀溶液中:H+(aq)+OH﹣(aq)=H2O(l);△H=﹣57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含l mol NaOH的溶液混合,放出的热量大于57.3kJ
D. 在25℃101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ的热量,则H2燃 烧的热化学方程式为:2H2(g)+O2(g)═2H2O(l);△H=﹣285.8kJ/mol
烧的热化学方程式为:2H2(g)+O2(g)═2H2O(l);△H=﹣285.8kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com