
ŃŠ¾æÄŃČܵē½āÖŹµÄ³ĮµķČܽāĘ½ŗā¼°ŌŚÉś²śÉś»īÖŠÓ¦ÓĆŅāŅåÖŲ“ó”£
£Ø1£©FeS³Įµķ·ĻĖ®ÖŠµÄHg2+µÄ·“Ó¦Ź½ĪŖ£ŗ_________________£»
£Ø2£©ĒāŃõ»ÆĶŠü×ĒŅŗÖŠ“ęŌŚČēĻĀĘ½ŗā£ŗCu(OH)2 (s) Cu2+(aq)+2OH-(aq£©£¬³£ĪĀĻĀĘäKsp=c£ØCu2+£©•c2£ØOH-£©=2”Į10-20mol2•L-2£»
Cu2+(aq)+2OH-(aq£©£¬³£ĪĀĻĀĘäKsp=c£ØCu2+£©•c2£ØOH-£©=2”Į10-20mol2•L-2£»
¢ŁÄ³ĮņĖįĶČÜŅŗĄļc(Cu2+)=0.02mol/L£¬ČēŅŖÉś³ÉCu(OH)2³Įµķ£¬Ó¦µ÷ÕūČÜŅŗpHŹ¹Ö®“óÓŚ_____£»
¢ŚŅŖŹ¹0.2mol/LĮņĖįĶČÜŅŗÖŠCu2+³Įµķ½ĻĪŖĶźČ«£ØŹ¹Cu2+ÅØ¶Č½µÖĮŌĄ“µÄĒ§·ÖÖ®Ņ»£©£¬ŌņÓ¦ĻņČÜŅŗĄļ¼ÓČėĒāŃõ»ÆÄĘČÜŅŗŹ¹ČÜŅŗÖŠOH-ÅضČĪŖ__________”£

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğø£½ØČżĆ÷Ņ»ÖŠøßŅ»ÉĻѧʌµŚ¶ž“ĪŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĪļÖŹÄÜÓĆĻąÓ¦µ„ÖŹÖ±½Ó»ÆŗĻ¶ųÖĘČ”µÄŹĒ
A£®FeS B£®FeCl2 C£®SO3 D£®NO2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğŗÓ±±Ź”ø߶žÉĻĘŚÖŠ²āŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
£Ø1£©¢ŁCaCO3£Øs£© == CaO£Øs£© + CO2£Øg£©£»¦¤H=177.7kJ/mol
¢ŚC£Øs£© + H2O£Øg£©== CO£Øg£© + H2£Øg£©£»¦¤H= -131.3kJ/mol
¢Ū0.5H2SO4£Øl£© + NaOH£Øl£© == 0.5Na2SO4£Øl£© + H2O£Øl£©£»¦¤H= -57.3kJ/mol
¢ÜC£Øs£© + O2£Øg£© == CO2£Øg£©£»¦¤H=-393.5kJ/mol
¢ŻCO£Øg£© + 1/2 O2£Øg£© == CO2£Øg£©£»¦¤H=-283kJ/mol
¢ŽHNO3 £Øaq£© + NaOH£Øaq£© == NaNO3£Øaq£© + H2O£Øl£©£»¦¤H= -57.3kJ/mol
¢ß2H2£Øg£© + O2£Øg£© == 2H2O£Øl£©£»¦¤H= -517.6kJ/mol
£Øa£©ÉĻŹöČČ»Æѧ·½³ĢŹ½ÖŠ£¬²»ÕżČ·µÄÓŠ
£Øb£©øł¾ŻÉĻŹöŠÅĻ¢£¬Š“³öC×Ŗ»ÆĪŖCOµÄČČ»Æѧ·½³ĢŹ½_ ”£
£Ø2£©ŅŃÖŖČČ»Æѧ·½³ĢŹ½£ŗH2£Øg£©+1/2O2£Øg£© === H2O£Øg£© ”÷H=£241.8kJ•mol-1£¬øĆ·“Ó¦µÄ»ī»ÆÄÜĪŖ167.2 kJ•mol-1£¬ŌņĘäÄę·“Ó¦µÄ»ī»ÆÄÜĪŖ 
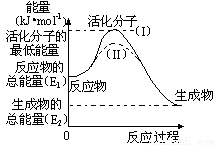
£Ø3£©ÓĆCH4“߻ƻ¹ŌNOxæÉŅŌĻū³żµŖŃõ»ÆĪļµÄĪŪČ¾”£ĄżČē£ŗ
CH4£Øg£©£«4NO2£Øg£©===4NO£Øg£©£«CO2£Øg£©£«2H2O£Øg£© ¦¤H£½£574 kJ”¤mol£1
CH4£Øg£©£«4NO£Øg£©===2N2£Øg£©£«CO2£Øg£©£«2H2O£Øg£©¦¤H£½£1 160 kJ”¤mol£1
ČōÓƱź×¼×“æöĻĀ4.48 L CH4»¹ŌNO2Éś³ÉN2£¬·“Ó¦ÖŠ×ŖŅʵĵē×Ó×ÜŹżĪŖ________£Ø°¢·ü¼ÓµĀĀŽ³£ŹżÓĆNA±ķŹ¾£©£¬·Å³öµÄČČĮæĪŖ________kJ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğĮÉÄžŹµŃé֊ѧ·ÖŠ£ø߶žÉĻ12ŌĀŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Óė±½»·ÉĻµÄĢ¼Ēā¼üĻą±Č£¬¼×±½ÖŠµÄ²ąĮ“¼×»ł»ņ±½·ÓÖŠµÄōĒ»ł¶Ō±½»·ÉĻµÄĢ¼Ēā¼üµÄ»Æѧ»īĘĆŠŌ¾ßÓŠ½Ļ“óÓ°Ļģ£¬ĻĀĮŠ¹ŲÓŚ¼×±½»ņ±½·ÓµÄŹµŃéŹĀŹµÖŠ£¬ÄÜĖµĆ÷²ąĮ“»ņōĒ»ł¶Ō±½»·ÓŠÓ°ĻģµÄŹĒ
A£®¼×±½ÄÜŹ¹ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ«
B£®¼×±½ÄÜÓėÅØĻõĖį”¢ÅØĮņĖį·“Ӧɜ³ÉTNT
C£®±½·ÓÄÜÓėFeCl3ČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦
D£®±½·Ó¾ßÓŠĖįŠŌ£¬ÄÜÓėĢ¼ĖįÄĘČÜŅŗ·¢Éś·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016Ń§ÄźÉ½Ī÷Ź”ø߶žÉĻ12ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŹŅĪĀĻĀ£¬Ä³°±Ė®pH=x£¬Ä³ŃĪĖįpH=y,ŅŃÖŖx+y=14£¬ĒŅx>11”£½«ÉĻŹö°±Ė®”¢ŃĪĖįµČĢå»ż»ģŗĻŗó£¬ĖłµĆČÜŅŗÖŠø÷ÖÖĄė×ÓÅضČÓɓ󵽊”µÄĖ³ŠņÕżČ·ŹĒ
A£®c£ØNH4+£©>c£ØCl-£©>c£ØOH-£©>c£ØH+£©
B£®c£ØCl-£©>c£ØNH4+£©>c£ØH+£©>c£ØOH-£©
C£®c£ØCl-£©=c£ØNH4+£©>c£ØOH-£©=c£ØH+£©
D£®c£ØCl-£©=c£ØNH4+£©>c£ØOH-£©>c£ØH+£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğĖēسɶ¼ĘßÖŠø߶žÉĻ12ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻņNa2CO3”¢NaHCO3»ģŗĻŅŗÖŠÖšµĪ¼ÓČėĻ”ŃĪĖį£¬Éś³ÉĘųĢåµÄĮæĖęĻ”ŃĪĖį¼ÓČėĮæµÄ±ä»Æ¹ŲĻµČēĶ¼£¬ŌņĻĀĮŠĄė×Ó×éŌŚ¶ŌÓ¦µÄČÜŅŗÖŠŅ»¶ØÄÜ“óĮæ¹²“ęµÄŹĒ
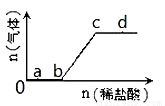
A£®aµć¶ŌÓ¦µÄČÜŅŗÖŠ£ŗCa2+”¢Mg2+”¢Br-”¢NO3-
B£®bµć¶ŌÓ¦µÄČÜŅŗÖŠ£ŗAl3+”¢Fe3+”¢MnO4-”¢NO3-
C£®cµć¶ŌÓ¦µÄČÜŅŗÖŠ£ŗNa+”¢Ca2+”¢NO3-”¢Cl-
D£®dµć¶ŌÓ¦µÄČÜŅŗÖŠ£ŗF-”¢NO3-”¢Fe2+”¢Ag+
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģŗžÄĻŹ”³¤É³ŹŠøßČżÉĻѧʌŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ģ¼ĖįĶŗĶ¼īŹ½Ģ¼ĖįĶ¾łæÉČÜÓŚŃĪĖį×Ŗ»ÆĪŖĀČ»ÆĶ”£øßĪĀĻĀÕāĮ½ÖÖ»ÆŗĻĪļ¾łÄÜ·Ö½ā³ÉŃõ»ÆĶ”£ŌŚøßĪĀĻĀÕāĮ½ÖÖ»ÆŗĻĪļ¾łÄÜ·Ö½ā³ÉŃõ»ÆĶ£®Čܽā28.4gÉĻŹö»ģŗĻĪļ£¬ĻūŗÄ1mol/LŃĪĖį500mL£®×ĘÉÕµČÖŹĮæµÄÉĻŹö»ģŗĻĪļ£¬µĆµ½Ńõ»ÆĶµÄÖŹĮæŹĒ
A£®35g B£®30g C£®20g D£®15g
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ¹ć¶«Ź”ø߶žÉĻĘŚÖŠ²āŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
»Æѧ·“Ó¦A2£Øg£©£«B2£Øg£©= 2AB£Øg£©µÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾£¬ĻĀĮŠÓŠ¹ŲŠšŹöÖŠÕżČ·µÄŹĒ( )
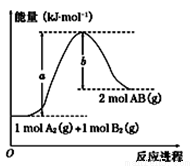
A£®ĆæÉś³É2 mol AB£Øg£©¹²ĪüŹÕb kJÄÜĮæ
B£®øĆ·“Ó¦ČȦ¤H£½£«£Øa£b£©KJ”¤mol£1
C£®·“Ó¦ĪļµÄ×ÜÄÜĮæ“óÓŚÉś³ÉĪļµÄ×ÜÄÜĮæ
D£®¶ĻĮŃ1 mol A”ŖA¼ü£¬·Å³öa kJÄÜĮæ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģŌĘÄĻŹ”øßČżÉĻµŚĖÄ“ĪŌĀæ¼Ąķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
”¾»Æѧ”Ŗ”ŖŃ”ŠŽ5 £ŗÓŠ»ś»Æѧ»ł“””æ
¹¤ŅµÉĻŗĻ³Éa£ŻĘĘ·“¼GµÄĀ·ĻßÖ®Ņ»ČēĻĀ£ŗ
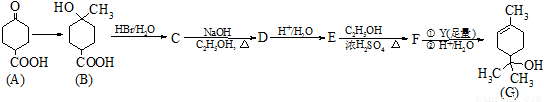
ŅŃÖŖ£ŗ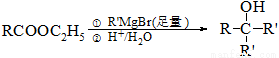
R”ŖOH +HBr H2O  R”ŖBr+ H2O
R”ŖBr+ H2O
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©FÖŠĖłŗ¬¹ŁÄÜĶŵÄĆū³ĘŹĒ £»B”śCµÄ·“Ó¦ĄąŠĶĪŖ ”£
£Ø2£©AµÄŗĖ“Ź²ÕńĒāĘ×ÓŠ øöĪüŹÕ·å£¬Ć껿±ČĪŖ ”£
£Ø3£©Š“³öC”śD×Ŗ»ÆµÄ»Æѧ·½³ĢŹ½ ”£
£Ø4£©Š“³öBŌŚŅ»¶ØĢõ¼žĻĀ¾ŪŗĻ³Éøß·Ö×Ó»ÆŗĻĪļµÄ»Æѧ·½³ĢŹ½ ”£
£Ø5£©GæÉŅŌÓėH2O“ß»Æ¼Ó³ÉµĆµ½»ÆŗĻĪļH£¬ĒėŠ“³öHæÉÄܵĽį¹¹¼ņŹ½£ØŠ“Ņ»ÖÖ¼“æÉ£© ”£
£Ø6£©Š“³öĶ¬Ź±Āś×ćĻĀĮŠĢõ¼žµÄEµÄĶ¬·ÖŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½ ”£
¢ŁÖ»ÓŠ3ÖÖ»·¾³µÄĒāŌ×Ó ¢ŚÄÜ·¢ÉśŅų¾µ·“Ó¦ ¢Ū·Ö×ÓÖŠŗ¬ĮłŌŖ»·
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com