
分析 (1)由亚硝酸钠能使血红蛋白中Fe2+转化为高铁血红蛋白而使人发生急性中毒,则亚硝酸钠具有氧化性,再由服用维生素C可解除NaNO2盐中毒,则解毒过程中Fe元素的化合价降低,维生素C中某元素的化合价升高,误食亚硝酸钠中毒,可服维生素C缓解,说明维生素C具有还原性,以此来解答;
(2)化合价升高元素在反应中被氧化;根据化学方程式转移电子的数目以及方程式的系数之间的关系来计算;
解答 解:亚硝酸钠能使血红蛋白中Fe2+转化为高铁血红蛋白而使人发生急性中毒,则亚硝酸钠具有氧化性,是氧化剂,Fe2+被氧化,误食亚硝酸钠中毒,可服维生素C缓解,说明维生素C具有还原性,
故答案为:氧化;氧化;还原;
(2)化合价升高的元素是H2O2中的O元素在反应中被氧化,反应2NaClO3+H2O2+H2SO4═2ClO2↑+O2↑+Na2SO4+2H2O中,有2mol电子转移,则产生的ClO2气体2mol,若反应中有0.1mol电子转移,则产生的ClO2气体0.1mol,在标准状况下的体积为0.1mol×22.4L/mol=2.24L,
故答案为:H2O2;2.24.
点评 本题以信息的形式考查氧化还原反应,把握反应中元素的化合价变化为解答的关键,注意习题中信息的应用,侧重氧化还原反应中基本概念的考查,题目难度不大.


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ③④⑤ | C. | ②③⑤ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 设计该循环是为了制取能源气体O2 | |
| B. | 整个循环过程中产生1 mol O2的同时产生44.8 L H2 | |
| C. | 图中反应Ⅰ、Ⅱ、Ⅲ均为氧化还原反应 | |
| D. | 图中反应Ⅰ、Ⅱ、Ⅲ均可在常温常压下进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向某溶液中加入少量硝酸银溶液,生成白色沉淀,说明原溶液中有Cl- | |
| B. | 向某溶液中加入少量氯化钡溶液,生成白色沉淀,说明原溶液中有SO42- | |
| C. | 向某溶液中加入少量氢氧化钙溶液,生成白色沉淀,说明原溶液中有CO32- | |
| D. | 向某溶液中加入足量盐酸,无现象,再加入少量BaCl2溶液,产生白色沉淀,说明原溶液中有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
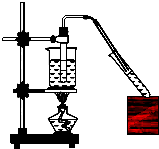 实验室用如图所示的装置制取乙酸乙酯.
实验室用如图所示的装置制取乙酸乙酯.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com