
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.标准状况下,等物质的量的C2H4和CH4所含的氢原子数均为4NA
B.1L0.4mol/L亚硫酸钠溶液中H2SO3、HSO3-、SO32-的总数为0.4NA
C.向含4molFeI2的溶液中通入等物质的量的Cl2,转移的电子数为4NA
D.100g98%的硫酸与磷酸的混合溶液中含氧原子数为0.4NA
【答案】B
【解析】
A.等物质的量的C2H4和CH4含有氢原子物质的量相同,但不一定是4mol,故A 错误;
B.1 L0.4mol/L亚硫酸钠溶液中溶质物质的量=1 L×0.4mol/L=0.4mol,亚硫酸根离子分步水解生成H2SO3、HSO3-,硫元素守恒得到溶液中H2SO3、HSO3-、SO32-的总数为0.4NA,故B 正确;
C.FeI2溶液中,碘离子的还原性大于亚铁离子的,通入氯气,先发生的反应为2I-+Cl2=I2+2Cl-~2mole-,则4molFeI2含8mol I-,由方程式得8molI-需要4molCl2,转移8mol电子,故通入4mol Cl2充分反应后转移的电子数为8NA,故C错误;
D.100g98%的硫酸与磷酸的混合液中中含有酸的物质的量为![]() =1mol,1mol酸含有4mol氧原子,溶液中水也含有氧原子,所以混合液中含有氧原子数大于4NA,故D错误;
=1mol,1mol酸含有4mol氧原子,溶液中水也含有氧原子,所以混合液中含有氧原子数大于4NA,故D错误;
故答案为B。


科目:高中化学 来源: 题型:
【题目】在生产生活和科学研究中,人们常常根据需要促进或抑制盐的水解。试回答下列问题:
(1)FeCl2溶液呈____(填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):____;实验室在配制FeCl2溶液时,常将FeCl2固体先溶于较浓的盐酸中,以_____(填“促进”、“抑制”)其水解,然后再用蒸馏水稀释到所需的浓度。
(2)用离子方程式表示硫酸铝溶液和碳酸氢钠溶液混合时发生的主要反应____。
(3)为证明盐的水解是吸热的,四位同学分别设计了如下方案,其中正确的是____。
A.甲同学:在盐酸中加入氨水,混合液温度上升,说明盐类水解是吸热的。 |
B.乙同学:将硝酸铵晶体溶于水,水温降低,说明盐类水解是吸热的。 |
C.丙同学:在氨水加入氯化铵固体,溶液的pH变小,说明盐类水解是吸热的。 |
D.丁同学:在醋酸钠溶液中滴加2滴酚酞试剂,加热后红色加深,说明盐类水解是吸热的。 |
(4)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃时,CaCO3饱和溶液中c(Ca2+)为5.3×10-5 mol·L-1 MgCO3的饱和溶液中c(Mg2+)为2.6×10-3 mol·L-1。若在5 mL浓度均为0.01 mol·L-1的CaCl2和MgCl2溶液中,逐滴加入5 mL 0.012 mol·L-1 Na2CO3溶液,充分反应后过滤得到溶液M和沉淀N(不考虑溶液体积的变化)。下列观点不正确的是
A.25℃时,Ksp(CaCO3)=2.8×10-9
B.加入Na2CO3溶液的过程中,先生成CaCO3沉淀
C.滤液M中:c(Cl-)>c(Na+)>c(Mg2+)>c(CO32-)>c(OH-)
D.滤液M中:![]() =
=
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁红(Fe2O3)和钛白粉(TiO2)均为重要的墙面装修颜料。一种利用钛铁矿(主要成分为FeTiO3,还含有少量Fe2O3)联合生产铁红和钛白粉的工艺流程如图所示:
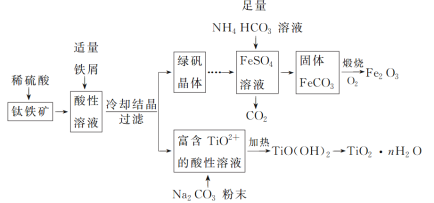
回答下列问题:
(1)FeTiO3中Fe的化合价为_______。
(2)为加快钛铁矿在稀硫酸中的溶解,可采取的措施有_______ (任写两种)。酸性溶液中加入适量铁屑的目的是将_______。
(3)FeSO4溶液与NH4HCO3溶液的反应温度应控制在35 ℃以下,其原因是_______,该反应的离子方程式是Fe2++2HCO3-=FeCO3↓+CO2↑+H2O。
(4)TiO2+转化为TiO(OH)2需要加热,加热的目的是_______,该反应的离子方程式为TiO2++2H2O![]() TiO(OH)2↓+2H+。
TiO(OH)2↓+2H+。
(5)常温时,在生成的FeCO3达到沉淀溶解平衡的溶液中,测得溶液中c(CO32-)=3.0×10-6 mol·L-1,pH为8.5,则所得的FeCO3中是否含Fe(OH)2_______?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨广泛用于生产化肥、制冷剂等方面。回答下列问题:
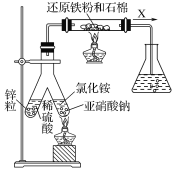
(1)实验室可用上图所示装置合成氨。
①亚硝酸钠与氯化铵反应的离子方程式为NO2-+NH4+![]() N2↑+2H2O。
N2↑+2H2O。
②锥形瓶中盛有一定量水并滴有几滴酚酞试剂。反应一段时间后,锥形瓶中溶液变红,则气体X的成分为N2、水蒸气、________和________(填化学式)。
(2)最近斯坦福大学研究人员发明了一种SUNCAT的锂循环系统,可持续合成氨,其原理如图所示。

①图中反应Ⅱ属于________(填“氧化还原反应”或“非氧化还原反应”)。
②反应Ⅲ中能量转化的方式是________(填“电能转变为化学能”或“化学能转变为电能”)。
(3)液氨可用作制冷剂,液氨汽化时________(填“释放”或“吸收”)能量;液氨泄漏遇明火会发生爆炸。已知部分化学键的键能数据如下表所示:
共价键 | N-H | O=O | N≡N | O-H |
键能/kJ·mol-1 | 391 | 498 | 946 | 463 |
则反应4NH3(g)+3O2(g)=2N2(g)+6H2O(g)的反应热ΔH=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,用水吸收SO2气体时,溶液中水的电离平衡________移动(填“向左”“向右”或“不”);若得到pH=4的H2SO3溶液,试计算溶液中![]() =________;SO2可用足量小苏打溶液吸收,反应的离子方程式是_________。(已知该温度下,H2SO3的电离常数:Ka1=4.5×10-2,Ka2=2.5×10-7,H2CO3的电离常数:Ka1=8.4×10-7,Ka2=1.2×10-10)
=________;SO2可用足量小苏打溶液吸收,反应的离子方程式是_________。(已知该温度下,H2SO3的电离常数:Ka1=4.5×10-2,Ka2=2.5×10-7,H2CO3的电离常数:Ka1=8.4×10-7,Ka2=1.2×10-10)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制硫酸的尾气中含有一定量SO2,处理尾气的手段除了氨吸收法以外还有以下几种方法。
(一)工业实际吸收过程中,第Ⅰ步常采用浓苛性钠溶液吸收为其中的SO2,然后向生成溶液中加入熟石灰,充分反应后将生成产物分离后再经氟化后制得产品A。
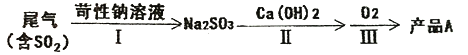
(1)产品A是_______(填化学式)。
(2)有人提出将第一步中的浓苛性钠溶液换成同温度下饱和Ca(OH)2溶液直接制得产品CaSO3,你认为是否可行?_______(填“可以”、“不可以”或“不确定”)原因是_______。
(二)制备MnSO4H2O:SO2还原MnO2矿制备MnSO4H2O,过程如下:

己知25℃时部分物质的溶度积常数如下表:
物质 | Mn(OH)2 | Fe(OH)3 | Cu(OH)2 | MnS | FeS | CuS |
溶度积 | 2.1×10-13 | 4.0× 10-38 | 2.2×10-23 | 1.0×10-11 | 6.3×10-18 | 6.3×10-38 |
(3)还原时,若尾气中SO2含量为4.48%,除去标况下lm3尾气至少需要含锰质量分数为55%的MnO2 矿粉_______g。
(4)除铁时加入碳酸钙,发生的反应的离子反应方程式为_____________________。
(5)试剂A最好是______________(写化学式)。
(6)操作I的名称为_________________。MnSO4H2O在1150℃高温下易分解,产物是Mn3O4、含硫化合物、水,在该条件下硫酸锰晶体分解反应的化学方程式是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国际社会发出落实《巴黎协定》,推动绿色低碳转型,构建人类命运共同体的积极信号。生态工业和循环经济成为综合解决人类资源、环境和经济发展的一条有效途径。
(1)水是“生命之基质”,是“永远值得探究的物质”。
以铂阳极和石墨阴极设计电解池,通过电解NH4HSO4溶液产生(NH4)2S2O8,再与水反应得到H2O2,其中生成的NH4HSO4可以循环使用。
①阳极的电极反应式是__。
②制备H2O2的总反应方程式是__。
(2)CO2的资源化利用能有效减少CO2排放,充分利用碳资源。
CO2催化加氢合成二甲醚是一种CO2转化方法,其过程中主要发生下列反应:
反应Ⅰ:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH=41.2kJ·mol1
反应Ⅱ:2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g) ΔH=-122.5kJ·mol1
在恒压、CO2和H2的起始量一定的条件下,CO2平衡转化率和平衡时CH3OCH3的选择性随温度的变化如图。其中:
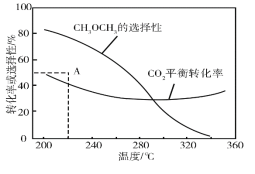
CH3OCH3的选择性=![]() ×100%
×100%
①温度高于300℃,CO2平衡转化率随温度升高而上升的原因是__。
②220℃时,在催化剂作用下CO2与H2反应一段时间后,测得CH3OCH3的选择性为48%(图中A点)。不改变反应时间和温度,一定能提高CH3OCH3选择性的措施有__。
废物再利用。如图装置加以必要的导线连接后达到利用粗铜精炼目的。
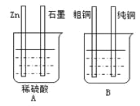
①A烧杯是__(填“电解池”或“原电池”)。
②其中Zn接B烧杯中的__,(填“粗铜”或“纯铜”),B烧杯中应该盛__溶液。
③分别写出石墨棒和纯铜棒的电极反应式
石墨棒:___,
纯铜棒:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,下列各组离子在指定溶液中一定能大量共存的是( )
A.0.1 mol·L-1 AlCl3溶液中:H+、Na+、Cl-、![]()
B.能使紫色石蕊溶液变蓝的溶液:Ag+、Fe3+、Br-、![]()
C.能使淀粉碘化钾试纸显蓝色的溶液:K+、![]() 、S2-、
、S2-、![]()
D.由水电离产生的c(H+)=10-12 mol·L-1的溶液中:![]() 、
、![]() 、
、![]() 、Cl-
、Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com