
| A. | 在基态多电子原子中,p轨道电子能量一定高于s轨道电子能量 | |
| B. | 基态Fe原子的外围电子排布图为 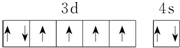 | |
| C. | 因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大 | |
| D. | 根据原子核外电子排布的特点,在Fe元素周期表中位于ds区 |
分析 A.同一层即同一能级中的p轨道电子的能量一定比s轨道电子能量高,但外层s轨道电子能量则比内层p轨道电子能量高;
B.基态铁原子外围电子排布式为3d64s2,根据洪特规则分析;
C.N原子的2p轨道处于半满,第一电离能大于氧原子;
D.Fe的外围电子排布式为3d64S2,位于元素周期表的d区.
解答 解:A.同一层即同一能级中的p轨道电子的能量一定比s轨道电子能量高,但外层s轨道电子能量则比内层p轨道电子能量高,故A错误;
B.基态铁原子外围电子排布式为3d64s2,根据洪特规则电子总是优先单独占据一个轨道,而且自旋状态相同,则外围电子排布图为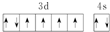 ,故B正确;
,故B正确;
C.N原子的2p轨道处于半满,第一电离能大于氧原子,故C错误;
D.Fe的外围电子排布式为3d64S2,位于元素周期表的d区,故D错误;
故选B.
点评 本题考查原子核外电子排布规律及排布式和排布图的书写,题目难度不大,本题注意原子核外电子的排布和运动特点.


科目:高中化学 来源: 题型:解答题
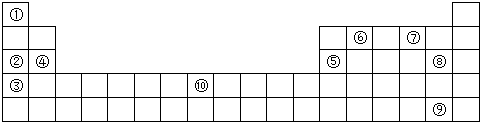
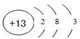 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液pH不断增大,最后为7 | B. | 阳极先析出Cl2,后析出O2 | ||
| C. | 阴极始终只析出H2 | D. | 电解最后阶段为电解水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
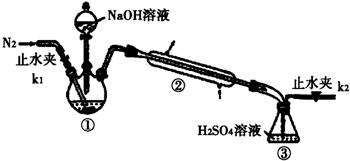
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 饱和Na2CO3溶液 | B. | NaOH稀溶液 | C. | 饱和Ca(OH)2溶液 | D. | CaCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
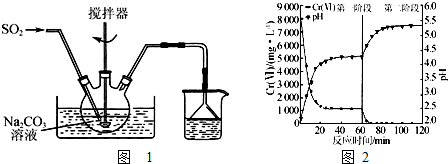
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇的球棍模型为: | B. | 次氯酸的结构式为:H一C1一O | ||
| C. | 淀粉的结构简式为:[C6H12O6]n | D. | 乙烯的电子式为: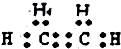 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com