
�⻯��ͭ(CuH)��һ����������,��CuSO4��Һ������һ��������40��50 ��ʱ��Ӧ����������CuH���ȶ�,�ֽ�;����������ȼ��;��ϡ���ᷴӦ����������;Cu+�����������·����ķ�Ӧ��2Cu+ Cu2++Cu������������Ϣ,����Լ������յĻ�ѧ֪ʶ,�ش�:
Cu2++Cu������������Ϣ,����Լ������յĻ�ѧ֪ʶ,�ش�:
(1)��CuSO4��Һ������һ��������CuH�ķ�Ӧ��,��������ԭ�۵����,������һ�������ڷ�Ӧ�������������������������������������
(2)д��CuH��������ȼ�յĻ�ѧ��Ӧ����ʽ
(3)CuH�ܽ���ϡ���������ɵ���������������,�����Ӧ�������˱�״����22.4 L������,����ԭ�����ӵõ��ӵ����ʵ���������������
(1)��ԭ����
(2)2CuH+3Cl2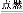 2CuCl2+2HCl��
2CuCl2+2HCl��
(3)H2��1.5 mol
��������(1)Cu2+ Cu+,ͭԪ�ػ��ϼ۽���,����ԭ,���Լ����Ӧ���ǻ�ԭ����
Cu+,ͭԪ�ػ��ϼ۽���,����ԭ,���Լ����Ӧ���ǻ�ԭ����
(2)CuH����������ȼ��,ͭԪ�غ���Ԫ�ض�����������,�ʿ���֪����Ϊ�Ȼ�ͭ���Ȼ���,���ݵ�ʧ�����غ��ԭ���غ�Ϳ�����ƽ��Ӧ����ʽ��
(3)CuH�ܽ���ϡ������,��Ԫ�ط������з�Ӧ,���ɵ�����Ϊ����,ͬʱ������ϢCu+�����������·����ķ�Ӧ��2Cu+ Cu2++Cu,���������ܻ�ѧ����ʽ��:2CuH+2HCl
Cu2++Cu,���������ܻ�ѧ����ʽ��:2CuH+2HCl CuCl2+Cu+2H2��,
CuCl2+Cu+2H2��,

������2 mol H2ʱ,ת�Ƶ���3 mol,����1 mol H2ʱ,ת�Ƶ���Ϊ1.5 mol��


 ��ĩ100�ִ��غ�������ϵ�д�
��ĩ100�ִ��غ�������ϵ�д� Сѧ�������Ծ�ϵ�д�
Сѧ�������Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014�߿���ѧ��ʦ֪ʶ�㾫�� ѡ��2��ѧ�뼼����ϰ���������棩 ���ͣ�ѡ����
��ѧ�뻷�������������,����������ȷ����(����)
A.��ɫ��ѧ�ĺ�����Ӧ�û�ѧԭ���Ի�����Ⱦ��������
B.ú��������Һ�����������仯����,�ɱ�Ϊ���ȼ��
C.PM2.5(2.5�����µĿ�����)����Ⱦ��Ҫ���Ի�ʯȼ�ϵ�ȼ��
D.�����������Դ,��ҵ�ϵ��ˮ���ƴ����������Ͻ��ܼ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ѧ��ʦ֪ʶ�㾫�� ר��7Ԫ�����ڱ���Ԫ����������ϰ���������棩 ���ͣ������
������Ԫ��A��B��C��D�����ڱ��е�λ����ͼ,E2+��D�ļ�����������ͬ�ĵ��Ӳ�ṹ,�ش���������:

(1)��A��B��C��D����Ԫ�ص�ԭ������֮��Ϊm,��m��������
A.һ��Ϊ����
B.һ��Ϊż��
C.����Ϊ����,Ҳ����Ϊż��
(2)DԪ��ԭ�ӵĴ������������������������֮��,��:
��д��A�γɵļ����ӵĽṹʾ��ͼ��������,Ԫ��Dλ��Ԫ�����ڱ��ĵ����������塣
��AԪ�ص�һ���⻯���������6��ԭ��,��ṹ��ʽΪ������������������ѹ298 Kʱ0.2 mol����̬�⻯����O2 ����ȫȼ��,������̬A���ʺ�ˮ,�ų�����106.8 kJ,����̬�⻯��ȼ�յ��Ȼ�ѧ����ʽΪ�� ����
��д��C������B������⻯�ﷴӦ�Ļ�ѧ����ʽ:
��ʵ��֤ʵAC3��ˮ�ᷢ����Ӧ����HNO2��HF,��AC3��NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ѧ��ʦ֪ʶ�㾫�� ר��5��ѧ����������ϰ���������棩 ���ͣ������
ͨ�����ǰѲ�1 molij��ѧ�������յ��������ɸû�ѧ���ļ��ܡ����ܵĴ�С���Ժ�����ѧ����ǿ��,Ҳ���Թ��㻯ѧ��Ӧ�ķ�Ӧ��(��H),��ѧ��Ӧ����H���ڷ�Ӧ�ж��Ѿɻ�ѧ���ļ���֮���뷴Ӧ���γ��»�ѧ���ļ���֮�͵IJ
��ѧ�� | Si��O | Si��Cl | H��H | H��Cl | Si��Si | Si��C |
����/kJ��mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
��ش���������:
(1)�Ƚ������������ʵ��۵�ߵ�(����>������<��)��
SiC��������Si;SiCl4��������SiO2��
(2)��ͼ���������ĵ�������ʾ�辧���е�һ��ԭ��,����������Ķ�����������ʾ����֮���ڵĹ�ԭ�ӡ�

(3)��ҵ���øߴ����ͨ�����з�Ӧ��ȡ:SiCl4(g)+2H2(g) Si(s)+4HCl(g),�÷�Ӧ�ķ�Ӧ����H=������kJ/mol��
Si(s)+4HCl(g),�÷�Ӧ�ķ�Ӧ����H=������kJ/mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ѧ��ʦ֪ʶ�㾫�� ר��5��ѧ����������ϰ���������棩 ���ͣ�ѡ����
��֪����ȼ�����ɶ�����̼��Һ̬ˮ�ų�������Ϊ55.625 kJ��g-1�������Ȼ�ѧ����ʽ�в���ȷ����(����)
A.CH4(g)+2O2(g) CO2(g)+2H2O(l) ��H =-890 kJ/mol
CO2(g)+2H2O(l) ��H =-890 kJ/mol
B.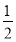 CH4(g)+O2(g)
CH4(g)+O2(g)
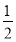 CO2(g)+H2O(l) ��H=-445 kJ/mol
CO2(g)+H2O(l) ��H=-445 kJ/mol
C.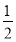 CO2(g)+H2O(l)
CO2(g)+H2O(l)
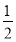 CH4(g)+O2(g) ��H=+445 kJ/mol
CH4(g)+O2(g) ��H=+445 kJ/mol
D.CH4(g)+2O2(g) CO2(g)+2H2O(l) ��H=-55.625 kJ/mol
CO2(g)+2H2O(l) ��H=-55.625 kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ѧ��ʦ֪ʶ�㾫�� ר��4������ԭ��Ӧ��ϰ���������棩 ���ͣ�ѡ����
�����й�˵����ȷ����(����)
A.1 mol Cl2�μӷ�Ӧת�Ƶ�����һ��Ϊ2NA
B.�ڷ�ӦKIO3+6HI KI+3I2+3H2O��,ÿ����3 mol I2ת�Ƶĵ�����Ϊ6NA
KI+3I2+3H2O��,ÿ����3 mol I2ת�Ƶĵ�����Ϊ6NA
C.���ݷ�Ӧ��HNO3(ϡ)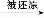 NO,��HNO3(Ũ)
NO,��HNO3(Ũ)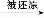 NO2��֪,������HNO3(ϡ)>HNO3(Ũ)
NO2��֪,������HNO3(ϡ)>HNO3(Ũ)
D.���д���NO3������Һ��,����ͬʱ��������H+��Fe2+��Cl-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ѧ��ʦ֪ʶ�㾫�� ר��3���ӷ�Ӧ��ϰ���������棩 ���ͣ������
ij�����Һ�п��ܺ��е��������±���ʾ:
���ܴ������е������� | H+��Ag+��Mg2+��Al3+��NH4+��Fe3+ |
���ܴ������е������� | Cl-��Br-��I-��CO32����AlO2�� |
Ϊ̽����ɷ�,����������̽��ʵ�顣
(1)̽��һ:
��ͬѧȡһ�����Ļ����Һ,��������μ�������������Һ,�������������ʵ���(n)���������������Һ�����(V)�Ĺ�ϵ��ͼ��ʾ��
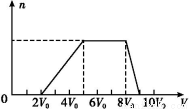
������Һ��һ�������ڵ����������� ,
һ�������ڵ�������������������������;���е����������Ӧ���ʵ���Ũ��֮��Ϊ�� ;
����д���������ٹ����з�����Ӧ�����ӷ���ʽ ��
(2)̽����:
��ͬѧ������Һ�к��д�����Cl-��Br-��I-,����1 L�û����Һ��ͨ��һ������Cl2,��Һ��Cl-��Br-��I-�����ʵ�����ͨ��Cl2�����(��״��)�Ĺ�ϵ���±���ʾ,������ش���������:
Cl2�����(��״��) | 11.2 L | 22.4 L | 28.0 L |
n(Cl-) | 2.5 mol | 3.5 mol | 4.0 mol |
n(Br-) | 3.0 mol | 2.5 mol | 2.0 mol |
n(I-) | x mol | 0 | 0 |
������ʼ��ͨ��Cl2�����Ϊ22.4 Lʱ,��Һ�з�����Ӧ�ܵ����ӷ���ʽΪ�� ;
��ԭ��Һ��Cl-��Br-��I-�����ʵ���Ũ��֮��Ϊ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ѧ��ʦ֪ʶ�㾫�� ר��2��ѧ��������Ӧ����ϰ���������棩 ���ͣ�ѡ����
��ͼ��ijѧУʵ���Ҵӻ�ѧ�Լ��̵���ص������Լ���ǩ�ϵIJ������ݡ��ݴ�����˵���������(����)

A.���������ǿ�ҵĸ�ʴ��,Ӧ����Σ�ջ�ѧ��Ʒ�������Ʊ���
B.ȡ10 mL���������ձ���,�ټ�18.4 mL��ˮ,�����49%������
C.����200 mL 4.6 mol/L��ϡ������ȡ������50 mL
D.���������������ˮ���������Һ�����ʵ���Ũ��С��9.2 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ѧ��ʦ֪ʶ�㾫�� ר��20ͬ���칹��Ӧ�����л��ϳ���ϰ���������棩 ���ͣ������
�㶹���������п������������ȶ���������ԡ��㶹�� 3
3 �������ˮ��ȩ
�������ˮ��ȩ
�Ʊ���
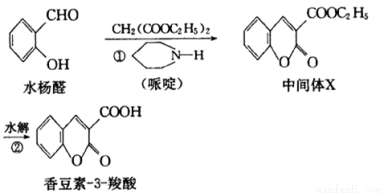
(1)�м���X�Ļ�ѧʽΪ����������
(2)ˮ��ȩ����������Ӧ�Ļ�ѧ����ʽΪ ����
(3)�㶹�� 3
3 ������NaOH��Һ�г���ˮ�����ɵ��л���Ľṹ��ʽΪ ��
������NaOH��Һ�г���ˮ�����ɵ��л���Ľṹ��ʽΪ ��
(4)����˵���д�����ǣ� ��
A.�м���X��������ˮ
B.ˮ��ȩ����������ԭ��һ������ͬһƽ��
C.ˮ��ȩ��������,���б���������������ͬ���칹�廹��4��
D.ˮ��ȩ���㶹�� 3
3 ���ᶼ��ʹ���Ը��������Һ��ɫ
���ᶼ��ʹ���Ը��������Һ��ɫ
(5)��Ӧ���еĴ�������ड������ɡ���ड��ϳ�,�䷴ӦΪ:
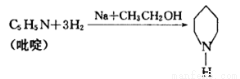
��֪���Ϊ��״,�����뱽���ơ�����वĽṹ��ʽΪ��������;��������(Ũ������Ũ��������)�ڼ���������,����������Ӧ���ɵ�ԭ�Ӽ�λ��һȡ����Ļ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com