
【题目】除去混合物中的杂质(括号中为杂质),所选试剂和分离方法都正确的是
混合物 | 除杂试剂 | 分离方法 | |
A | 乙烷(乙烯) | Br2(CCl4) | 洗气 |
B | 乙醇(水) | 生石灰 | 过滤 |
C | 硝基苯(HNO3) | NaOH溶液 | 分液 |
D | 溴苯(溴) | CCl4 | 萃取 |
A.AB.BC.CD.D
科目:高中化学 来源: 题型:
【题目】草酸钴是制作氧化钴和金属钴的原料,一种利用含钴废料(主要成分为Co2O3,含少量Fe2O3、ZnO、Al2O3、CaO、MgO、碳及有机物等)制取CoC2O4的工艺流程如下:
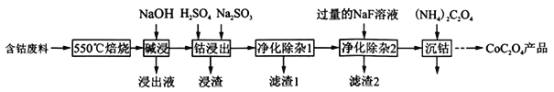
已知:ZnO与Al2O3化学性质相似,既能溶于强酸又能溶于强碱
(1)“550℃焙烧”的目的是______________________;
(2)“浸出液”的主要成分是_____________________;
(3)“钴浸出”过程中Co3+转化为Co2+,反应的离子方程式为_____________________;
(4) “净化除杂1”过程中,先在40 ~ 50℃加入H2O2,其作用是____________________ (用离子方程式表示);再升温至80~85℃,加入___________溶液,调pH至4.5以达到净化除杂的目的。
(5)“净化除杂2”过程中,若溶液c(Ca2+)=0.01mol/L,使Mg2+恰好沉淀完全即溶液中c(Mg2+)=1.0×10-5mol/L,此时是否有CaF2沉淀生成________________?(列式计算)[已知Ksp(MgF2) =7.0×10-11、Ksp(CaF2) =1.0×10-10]。
(6)为测定制得样品的纯度,现称取1.000g样品,将其用适当试剂转化,得到草酸铵[(NH4)2C2O4]溶液,再用过量稀硫酸酸化,用0. 1000 mol/L KMnO4溶液滴定,达到滴定终点时,共用去KMnO4溶液26.00 mL,则草酸钴样品的纯度为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列各说法中,正确的是
A. 对于2SO2(g)+O2(g) ![]() 2SO3(g) ΔH=-Q kJ·mol-1,(Q>0),若反应中充入1mol SO2和足量的氧气反应时,放出的热量一定是Q/2 kJ
2SO3(g) ΔH=-Q kJ·mol-1,(Q>0),若反应中充入1mol SO2和足量的氧气反应时,放出的热量一定是Q/2 kJ
B. 热化学方程式中的化学计量数不能用分数表示
C. Zn(s)+H2SO4(aq) ===ZnSO4(aq)+H2(g) ΔH<0,该反应的化学能可以转化为电能
D. ΔH的大小与热化学方程式的化学计量数无关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将晶体X加热分解,可得A、B、D、E、F和H2O六种产物,其中A、B、D都是中学化学中常见的氧化物,气体E是单质F所含元素的氢化物。
(1) A能溶于强酸、强碱,写出A与强碱溶液反应的离子方程式: ________________________。
(2)B、D都是酸性氧化物且组成元素相同,D溶于水得强酸,则B、D分子中除氧元素外所含另一种元素在元素周期表中的位置是____________________。
(3)E能使湿润的红色石蕊试纸变蓝,E的结构式为__________________,工业制取E气体的化学方程式为___________________________。
(4)由各分解产物的物质的量之比推测X的组成类似于明矾,若向X的浓溶液中滴加浓NaOH溶液至过量,现象依次为____________________、____________________、__________________。
(5)取一定量的X晶体分解,若生成0.1mol F,则必同时生成____________(填化学式)________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外兴趣小组用右图装置进行实验,试回答:
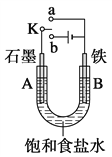
(1)若开始时开关K与a连接,则A电极反应式为___________________。
(2)若开始时开关K与b连接,这种方法经常用于金属的防护,这种防护措施叫做________________,则A电极反应式为_____________________;B电极反应式为_________________________。
(3)开关K与b连接,将饱和食盐水换成CuSO4溶液,则A电极反应式为___________,该反应的离子方程式为______________________________ ,电解一段时间后(溶液仍然为蓝色),溶液的pH值将_________(填“变大”、“变小”、“不变”),若将电解质溶液恢复至原状,应补充_____________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨及其相关工业中,部分物质间的转化关系如下:

下列说法正确的是
A. 反应I、Ⅱ、Ⅲ、V均属于氧化还原反应
B. 甲、乙、丙和丁四种物质中都含有氮元素
C. 反应Ⅳ和Ⅵ中的部分产物可在上述流程中循环利用
D. 反应V是先向饱和氯化钠溶液中通CO2至饱和再通NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】核糖是合成核酸的重要原料之一,其结构简式为CH2OH—CHOH—CHOH—CHOH—CHO,下列关于核糖说法正确的是
A.能发生还原反应
B.能发生水解反应
C.能与NaOH反应
D.与葡萄糖互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气溶于水,Cl2约有三分之一与水反应生成盐酸与次氯酸。请回答下列问题:
(1)该可逆反应的离子方程式为__________________。
(2)氯气____溶于饱和食盐水,其原因是增大了上述平衡中的_____浓度,平衡向___反应方向移动。
(3)在上述平衡体系中加入少量NaOH固体,平衡将向______反应方向移动;
(4)如果增大氯气的压强,氯气在水中的溶解度将_______(填“增大”、“减小”或“不变”),平衡将向_______反应方向移动。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com