
| A£® | »ī»ÆÄܵē󊔶Ō»Æѧ·“Ó¦µÄÄÜĮæ±ä»Æ²»²śÉśÓ°Ļģ | |
| B£® | »Æѧ¼üµÄ¶ĻĮŃŗĶŠĪ³ÉŹĒ»Æѧ·“Ó¦ÖŠ·¢ÉśÄÜĮæ±ä»ÆµÄÖ÷ŅŖŌŅņ | |
| C£® | HCl£Øaq£©ŗĶNaOH£Øaq£©·“Ó¦µÄÖŠŗĶČČĪŖ57.3 kJ/mol£¬ŌņCH3COOH£Øaq£©ŗĶNaOH£Øaq£©ĶźČ«·“Ӧɜ³É1 mol H2O£Øl£©Ź±£¬·Å³öµÄČČĮæĪŖ57.3 kJ | |
| D£® | CO£Øg£©µÄČ¼ÉÕČČŹĒ283.0 kJ/mol£¬Ōņ·“Ó¦2CO2£Øg£©=2CO£Øg£©+O2£Øg£©µÄ·“Ó¦ČČ”÷H=+566.0kJ/mol |
·ÖĪö A”¢»ī»ÆÄܵē󊔶Ō·“Ó¦µÄÄŃŅ׳Ģ¶ČÓŠÓ°Ļģ£»
B”¢øł¾Ż»Æѧ·“Ó¦ÖŠ·¢ÉśÄÜĮæ±ä»ÆµÄÖ÷ŅŖŌŅņŹĒ»Æѧ¼üµÄ¶ĻĮŃŗĶŠĪ³É£»
C”¢CH3COOHŹĒČõĖįµēĄėĪüČČ£»
D”¢COČ¼ÉÕ·ÅČČ£¬Ōņ·“Ó¦2CO2 £Øg£©=2CO£Øg£©+O2£Øg£©ĪüČČ£®
½ā“š ½ā£ŗA”¢»ī»ÆÄܵē󊔶Ō·“Ó¦µÄÄŃŅ׳Ģ¶ČÓŠÓ°Ļģ£¬¶Ō»Æѧ·“Ó¦Ē°ŗóµÄÄÜĮæ±ä»Æ²»²śÉśÓ°Ļģ£¬¹ŹAÕżČ·£»
B”¢»Æѧ±ä»ÆµÄŹµÖŹĪŖ¾É¼ü¶ĻĮŃŗĶŠĀ¼üŠĪ³É£¬Ōņ»Æѧ¼üµÄ¶ĻĮŃŗĶŠĪ³ÉŹĒ»Æѧ·“Ó¦ÖŠÄÜĮæ±ä»ÆµÄÖ÷ŅŖŌŅņ£¬¹ŹBÕżČ·£»
C”¢CH3COOHŹĒČõĖįµēĄėĪüČČ£¬·Å³öµÄČČĮæŠ”ÓŚ57.3kJ£¬¹ŹC“ķĪó£»
D”¢CO£Øg£©µÄČ¼ÉÕČČŹĒ283.0kJ/mol£¬Ōņ±ķŹ¾Č¼ÉÕČȵÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗCO£Øg£©+$\frac{1}{2}$O2£Øg£©ØTCO2£Øg£©”÷H=-283.0kJ/mol£¬µ±·½³ĢŹ½·“Š“”÷H·ūŗÅĻą·“£¬¼ĘĮæŹż±ä»Æ¼ø±¶”÷HŅ²ŅŖ±ä»Æ¼ø±¶£¬ĖłŅŌ2CO2£Øg£©ØT2CO£Øg£©+O2£Øg£©·“Ó¦µÄ”÷H=+2”Į283.0kJ/mo=+566.0kJ/moll£¬¹ŹDÕżČ·£®
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éÄÜĮæµÄ×Ŗ»»ŠĪŹ½£¬ÖŠŗĶČČŅŌ¼°Č¼ÉÕČȵÄøÅÄī£¬×¢Ņā×¼Č·°ŃĪÕČ¼ÉÕČȵÄøÅÄī£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ¶Ō“ĖÓŠ»śĪļµÄĻĀĮŠŠšŹöÖŠ£¬ÕżČ·µÄŹĒ£Ø””””£©
¶Ō“ĖÓŠ»śĪļµÄĻĀĮŠŠšŹöÖŠ£¬ÕżČ·µÄŹĒ£Ø””””£©| A£® | ŌŚøĆÓŠ»śĪļ·Ö×ÓÖŠ£¬½öŗ¬ÓŠŅ»ÖÖ¹ŁÄÜĶÅ | |
| B£® | ŌŚŅ»¶ØĢõ¼žĻĀøĆ1molÓŠ»śĪļæÉÓė2molH2·¢Éś¼Ó³É·“Ó¦ | |
| C£® | øĆÓŠ»śĪļÄÜŌŚČĪŗĪĢõ¼žĻĀ¶¼²»ÄÜ·¢ÉśČ”“ś·“Ó¦ | |
| D£® | øĆÓŠ»śĪļÄÜÓėŅų°±ČÜŅŗ·¢ÉśŅų¾µ·“Ó¦£¬µ«²»ÄÜŹ¹ĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆ¼¤¹ā±Ź¼ų±šµķ·ŪČÜŅŗÓėĀČ»ÆÄĘČÜŅŗ | |
| B£® | ÓĆKOHČÜŅŗ¼ų±šNH4Cl”¢AlCl3”¢MgSO4”¢FeCl3ĖÄÖÖČÜŅŗ | |
| C£® | ÓĆŃĪĖįČÜŅŗ¼ų±šNa2CO3ČÜŅŗŗĶNa2SiO3ČÜŅŗ | |
| D£® | ÓĆBaCl2ČÜŅŗ¼ų±šAgNO3ŗĶNa2SO4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1 mol CO2µÄĢå»żŹĒ22.4L | B£® | 1 mol NaClµÄÖŹĮæŹĒ58.5 | ||
| C£® | H2SO4µÄĦ¶ūÖŹĮæŹĒ98 g/mol | D£® | 1 mol/L NaOHČÜŅŗÖŠŗ¬ÓŠ1 molNa+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | HCl | B£® | KOH | C£® | NaCl | D£® | CuSO4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ÄÉĆ×¼¶¶žŃõ»ÆĆĢµÄ»īŠŌŗÜøߣ¬ŅŌ¶žŃõ»ÆĆĢĪŖµē¼«¹¹³ÉµÄČ¼ĮĻµē³ŲČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ £Ø””””£©
ÄÉĆ×¼¶¶žŃõ»ÆĆĢµÄ»īŠŌŗÜøߣ¬ŅŌ¶žŃõ»ÆĆĢĪŖµē¼«¹¹³ÉµÄČ¼ĮĻµē³ŲČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ £Ø””””£©| A£® | a¼«ĪŖÕż¼«£¬·¢Éś»¹Ō·“Ó¦ | |
| B£® | b¼«µÄµē¼«·“Ó¦Ź½ĪŖ£ØCH2O£©n-4ne-+n H2O=nCO2+4n H+ | |
| C£® | µē×ÓÓÉb¼«Į÷³ö¾ÓƵēĘ÷Į÷Ļņa¼« | |
| D£® | ·ÅµēŹ±H+ÓÉÖŹ×Ó½»»»Ä¤×ó²ąĻņÓŅ²ąĒØŅĘ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĒāŃõ»Æ±µČÜŅŗÓėĻ”ĮņĖį·“Ó¦£ŗBa2++SO42-+H++OH-=BaSO4”ż+H2O | |
| B£® | ĶłĢ¼ĖįĆ¾ÖŠµĪ¼ÓĻ”ŃĪĖį£ŗCO32-+2H+=CO2”ü+H2O | |
| C£® | Ķł³ĪĒåŹÆ»ŅĖ®ÖŠĶØČė¹żĮ涞Ńõ»ÆĢ¼£ŗCa2++2OH-+CO2=CaCO3”ż+H2O | |
| D£® | ÓĆŠ”ĖÕ“ņÖĪĮĘĪøĖį¹ż¶ą£ŗHCO3-+H+=CO2”ü+H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŃÖŖ2H2£Øg£©+O2£Øg£©=2H2O£Øg£©”÷H=-483.6 kJ•mol-1ŌņĒāĘųµÄČ¼ÉÕČČĪŖ241.8 kJ•mol-1 | |
| B£® | ŅŃÖŖC£ØŹÆÄ«£¬s£©=C£Ø½šøÕŹÆ£¬s£©”÷H£¾0””Ōņ½šøÕŹÆ±ČŹÆÄ«µÄ¼üÄÜ“ó | |
| C£® | ŅŃÖŖNaOH£Øag£©+HCl£Øaq£©=NaCl£Øaq£©+H2O£Øl£©”÷H=-57.4 kJ•mol-1Ōņŗ¬20.0g NaOHµÄĻ”ČÜŅŗÓėĻ”ŃĪĖįĶźČ«ÖŠŗĶ£¬·Å³ö28.7kJµÄČČĮæ | |
| D£® | ŅŃÖŖ2C£Øs£©+2O2£Øg£©=2CO2£Øg£©”÷H1 2C£Øs£©+O2£Øg£©=2CO£Øg£©”÷H2£¬Ōņ”÷H1£¾”÷H2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  | B£® | 26M3+ | C£® | 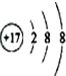 | D£® | 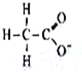 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com