
| A. | 需要加热才发生的化学反应,反应物的总能量可能高于生成物的总能量 | |
| B. | 已知:H2(g)+F2(g)═2HF(g)△H=-270 kJ•mol-1,则1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ | |
| C. | 500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)═2NH3(g)△H=-38.6 kJ•mol-1 | |
| D. | 已知:C(s,金刚石)═C(s,石墨)△H=-1.5 kJ•mol-1,说明金刚石更稳定 |
分析 A、化学反应是否加热才能进行与反应热无关;
B、液态氟化氢的能量比气态氟化氢的能量低,根据能量守恒;
C、根据可逆反应的特点:反应物不能完全转化为产物来回答;
D、能量越高越不稳定.
解答 解:A、持续加热的条件才能发生的反应是吸热反应,所以需要加热才发生的化学反应,反应物的总能量可能高于生成物的总能量,如铝热反应在高温下才能进行,但属于放热反应,故A正确;
B、液态氟化氢的能量比气态氟化氢的能量低,根据能量守恒,1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量大于270kJ,故B错误;
C、根据可逆反应的特点:反应物不能完全转化为产物,0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,1mol N2和3molH2置于密闭的容器中充分反应生成NH3(g),放热小于38.6kJ,故C错误;
D、C(s,金刚石)═C(s,石墨)△H=-1.5 kJ•mol-1,说明金刚石能量高,能量越高越不稳定,所以石墨更稳定,故D错误;
故选A.
点评 本题是一道涉及反应热和焓变知识的综合考查题,考查学生对基础知识的梳理和应用情况,难度中等.


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:选择题
| 物质 | 杂质 | 试剂 | 主要操作 | |
| A | SiO2 | Fe2O3 | 盐酸 | 过滤 |
| B | Mg | Al | NaOH | 过滤 |
| C | FeCl2 | FeCl3 | Cu | 过滤 |
| D | KNO3 | KCl | H2O | 冷却结晶 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯无同分异构体 | B. | 间二甲苯没有同分异构体 | ||
| C. | 邻二甲苯没有同分异构体 | D. | 1 mol苯只能与3 molH2加成 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 氢氧化钠溶液、碳酸钠溶液、氯化钡溶液 | |
| B. | 氢氧化钠溶液、氯化钡溶液、碳酸钠溶液 | |
| C. | 氯化钡溶液、碳酸钠溶液、氢氧化钠溶液 | |
| D. | 碳酸钠溶液、氯化钡溶液、氢氧化钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑥ | B. | ①②③④⑥ | C. | ①②③⑥ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 小于 (0.1+a) mol•L-1 | B. | 大于 (0.1+a) mol•L-1 | ||
| C. | 等于 (0.1+a) mol•L-1 | D. | 等于2a mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
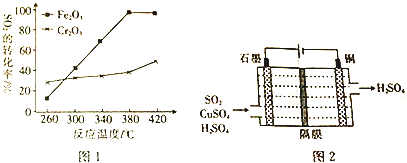
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Na+2H2O═2NaOH+H2↑ | B. | MnO2+4HCl(浓)═MnCl2+2H2O+Cl2↑ | ||
| C. | Na2CO3+CO2+H2O═2NaHCO3 | D. | 2Na2O2+2CO2═2Na2CO3+O2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com