

| A.高温、高压 | B.适宜温度、高压、催化剂 |
| C.低温、低压、不断分离出甲醇 | D.低温、高压、催化剂 |
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源:不详 题型:单选题
 eC(气)+fD(气),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是
eC(气)+fD(气),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是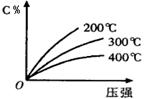
| A.达到平衡后,加入催化剂,C%不变 |
| B.该反应为放热反应 |
| C.化学方程式中m+n>e+f |
| D.达到平衡后,增加A的质量有利于平衡向右移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2C(g), 达到平衡时B的浓度为0.1mol/L,则A的转化率为 ( )
2C(g), 达到平衡时B的浓度为0.1mol/L,则A的转化率为 ( )| A.67% | B.50% | C.25% | D.缺少条件无法计算 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2HI(g)已经达到平衡状态的是
2HI(g)已经达到平衡状态的是| A.①③ | B.②⑥ | C.③⑥ | D.④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 pC(g)反应平衡时,测得c(A)为0.5 mol·L-1,在温度不变的情况下,将容器体积增大一倍,当达到新的平衡时,测得c(A)为0.3 mol·L-1,则下列判断中正确的是
pC(g)反应平衡时,测得c(A)为0.5 mol·L-1,在温度不变的情况下,将容器体积增大一倍,当达到新的平衡时,测得c(A)为0.3 mol·L-1,则下列判断中正确的是查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.饱和氯水中加水稀释,促进氯水中水的电离 |
| B.向氨水中加入氯化铵,由于氯化铵溶液呈酸性,所以溶液pH降低 |
C.碳酸钠溶液中存在CO32-+H2O  HCO3-+OH-平衡,若通入CO2,则平衡逆向移动 HCO3-+OH-平衡,若通入CO2,则平衡逆向移动 |
| D.向氢氧化镁悬浊液中加水稀释,Mg(OH)2沉淀溶解平衡正向移动,但c(Mg2+)降低 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2HI(g)正反应为放热反应,改变下列条件,反应速率将如何改变(填增大、减小、或不变),平衡将如何改变(填向左、向右或不)
2HI(g)正反应为放热反应,改变下列条件,反应速率将如何改变(填增大、减小、或不变),平衡将如何改变(填向左、向右或不)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2HI(g)△ H<0,并达到平衡,HI的体积分数ω(HI)随时间变化如图(Ⅱ)所示。若改变反应条件, ω(HI)的变化曲线如图(Ⅰ)所示,则改变的条件可能是
2HI(g)△ H<0,并达到平衡,HI的体积分数ω(HI)随时间变化如图(Ⅱ)所示。若改变反应条件, ω(HI)的变化曲线如图(Ⅰ)所示,则改变的条件可能是 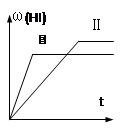
| A.恒温恒容条件下,加入适当催化剂 |
| B.恒温条件下,缩小反应容器体积 |
| C.恒容条件下升高温度 |
| D.恒温条件下,扩大反应容器体积 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com