
分析 (1)金属离子全部沉淀时,得到25.4g沉淀为氢氧化铜、氢氧化镁,故沉淀中氢氧根的质量为25.4g-15.2g=10.2g,根据n=$\frac{m}{M}$计算氢氧根的物质的量,根据电荷守恒可知,金属提供的电子物质的量等于氢氧根的物质的量,令铜、镁合金中Cu、Mg的物质的量分别为xmol、ymol,根据提供的电子物质的量与二者质量之和列方程计算x、y的值,据此解答;
(2)根据c=$\frac{1000ρω}{M}$计算该浓硝酸的物质的量浓度;
(3)根据n=$\frac{V}{{V}_{m}}$计算NO2和N2O4混合气体的物质的量,互为二氧化氮的物质的量为xmol,根据电子转移列放出计算;
(4)根据钠离子守恒可知,氢氧化钠的物质的量等于反应后溶液中硝酸钠的物质的量,根据氮元素守恒计算硝酸钠的物质的量,再根据V=$\frac{n}{c}$计算需要氢氧化钠溶液的体积.
解答 解:(1)金属离子全部沉淀时,得到25.4g沉淀为氢氧化铜、氢氧化镁,故沉淀中氢氧根的质量为25.4g-15.2g=10.2g,氢氧根的物质的量为:$\frac{10.2g}{17g/mol}$=0.6mol,根据电荷守恒可知,金属提供的电子物质的量等于氢氧根的物质的量,设铜、镁合金中Cu、Mg的物质的量分别为xmol、ymol,
则:$\left\{\begin{array}{l}{2x+2y=0.6}\\{64x+24y=15.2}\end{array}\right.$,
解得:x=0.2\y=0.1,故合金中铜与镁的物质的量之比是0.2mol:0.1mol=2:1,
故答案为:2:1;
(2)该浓硝酸密度为1.40g/mL、质量分数为63%,故该浓硝酸的物质的量浓度为:$\frac{1000×1.40×63%}{63}$mol/L=14mol/L,
故答案为:14mol/L;
故答案为:14mo/L;
(3)NO2和NO混合气体的总物质的量为:$\frac{11.2L}{22.4L/mol}$=0.5mol,设二氧化氮的物质的量为xmol,则NO的物质的量为(0.5-x)mol,
根据电子转移守恒可知,x×1+(0.5-x)×3=0.6,解得:x=0.45,则NO的物质的量为:0.5mol-0.4mol=0.05mol,
所以NO2和NO的物质的量的比是0.45mol:0.05mol=9:1,
故答案为:9:1;
(4)根据钠离子守恒可知,氢氧化钠的物质的量等于反应后溶液中硝酸钠的物质的量,根据氮元素守恒可知,硝酸钠的物质的量为0.1L×14mol/L-0.5mol=0.9mol,故需要氢氧化钠溶液的体积为:$\frac{0.9mol}{1mol/L}$=0.9L=900mL,
故答案为:900.
点评 本题考查混合物反应的有关计算,题目难度中等,理解反应发生的过程是关键,是对学生综合能力的考查,注意根据守恒思想进行的解答,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:解答题
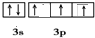 .
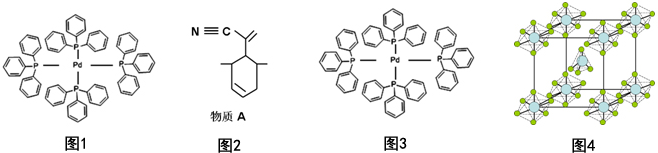
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①② | B. | 只有②③ | C. | 全部 | D. | 只有③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在船舶的外壳装上镁合金或锌块保护钢铁设备被称为牺牲阳极的阴极保护法 | |
| B. | 赤潮、白色污染、绿色食品中的“赤”“白”“绿”均指相关物质的颜色 | |
| C. | 海水淡化的方法主要有:蒸馏法、电渗析法、离子交换法等 | |
| D. | 乙烯的产量可以用来衡量一个国家的石油化工发展水平 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca(OH)2溶液 | B. | 浓的CaCl2溶液 | C. | Ba(NO3)2溶液 | D. | H2S的水溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向含3mol次氯酸钠溶液中通入1mol二氧化硫:3ClO-+H2O+SO2═2HClO+SO4-+Cl- | |
| B. | 向碳酸氢钠溶液中加入过量氢氧化钙溶液2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- | |
| C. | 氢氧化钡溶液与硫酸溶液反应得到中性溶液Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | 50mL1mol/L的FeI2溶液中通入0.05molCl2:2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
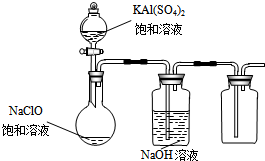 NaClO和KAl(SO4)2都是重要的化工产品,均可应用于造纸业.
NaClO和KAl(SO4)2都是重要的化工产品,均可应用于造纸业.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHSO4在熔融状态下的电离方程式为NaHSO4═Na++H++SO42- | |
| B. | H2CO3是弱酸,故Na2CO3是弱电解质 | |
| C. | Fe3O4俗称铁红,常用作红色油漆和涂料 | |
| D. | 2.4 g Mg无论与O2还是与N2完全反应转移的电子数均为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌与镁 | B. | 铁与锌 | C. | 铝与铁 | D. | 镁与铁 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com