
分析 NaClO具有强氧化性,Na2S2具有还原性,二者反应生成NaCl、Na2SO4,其反应方程式为Na2S2+7NaClO+2NaOH=2Na2SO4+7NaCl+H2O,结合化合价的变化计算电子转移.
解答 解;NaClO具有强氧化性,Na2S2具有还原性,二者反应生成NaCl、Na2SO4,其反应方程式为Na2S2+7NaClO+2NaOH=2Na2SO4+7NaCl+H2O,反应中转移电子数目为14,用单线桥标明电子转移情况为: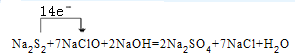 ;
;
故答案为: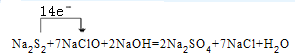 .
.
点评 本题考查氧化还原反应判断、电子转移方向和数目的书写,侧重考查基本概念,熟悉常见元素化合价变化,注意把握单线桥法表示电子转移,题目难度不大.


科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在水溶液里或熔融状态下能够导电的物质叫做电解质 | |
| B. | 微粒直径在10-9 m-10-7m之间的分散系为胶体 | |
| C. | 能够电离出氢离子的化合物叫酸 | |
| D. | 胶体区别于其他分散系的本质特征是具有丁达尔效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ③②① | C. | ②③① | D. | ②①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 实验序号 | 操作 | 现象 |
| 实验一 | 关闭弹簧夹,滴加一定量浓硫酸,加热 | A中: (I)加热初期,Cu片表面变黑,溶液近乎无色 (II)继续加热,铜片表面产生气泡,形成黑色浊液,三口瓶底部有灰黑色固体沉积 (III)继续加热,有大量白雾生成,浊液变澄清,三口瓶底部有大量白色固体(因含有极少量黑色固体而显灰白色),Cu片消失B中有气泡冒出,溶液褪色 |
| 实验二 | 停止加热,冷却,将三口瓶中的上清液倒入盛有水的烧杯中 | 三口瓶中留有大量白色固体(因含有极少量黑色固体而显灰白色) 烧杯中溶液温度升高,溶液只略带蓝色 |

查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 有机物A是一种含溴的酯,分子式为C6H9O2Br.已知A有如下的转化关系:
有机物A是一种含溴的酯,分子式为C6H9O2Br.已知A有如下的转化关系:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ③④⑤ | C. | ①②④ | D. | ①③⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com