
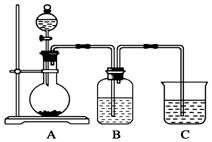
 某同学设计实验以探究元素性质的递变规律,实验装置如图所示.
某同学设计实验以探究元素性质的递变规律,实验装置如图所示.分析 实验Ⅰ:元素最高价含氧酸的酸性强弱判断元素非金属性强弱,酸性越强,非金属性越强,A中反应是碳酸钙和稀硝酸反应生成二氧化碳,证明氮非金属性大于碳;B装置是为了吸收挥发出的硝酸蒸气,避免证明碳的非金属性大于硅的实验,C中为Na2SiO3溶液,二氧化碳通入反应生成硅酸沉淀,证明碳的非金属性大于硅.
(1)A中反应是碳酸钙和稀硝酸反应生成二氧化碳,证明氮非金属性大于碳;C中为Na2SiO3溶液,二氧化碳通入反应生成硅酸沉淀,证明碳的非金属性大于硅;
(2)B装置是为了吸收挥发出的硝酸蒸气,避免证明碳的非金属性大于硅的实验;
(3)根据实验现象和元素最高价含氧酸的酸性强弱判断元素非金属性强弱,酸性越强,非金属性越强,推知C、N、Si三种元素非金属性的强弱;
实验Ⅱ:探究氯、溴的非金属性强弱的递变规律,根据实验装置图可知,实验原理为A装置:浓盐酸与高锰酸钾反应生成氯气,氯气通入装置B:溴化钾溶液中,溶液出现红色,有溴单质生成,说明氯的非金属性强于溴,装置中挥发出来的溴或氯气都有毒,会污染空气,所以要用装置C:氢氧化钠溶液吸收,据此分析.
解答 解:实验Ⅰ:(1)A中反应是碳酸钙和稀硝酸反应生成二氧化碳,反应的离子方程式为:CaCO3+2H+=Ca2++CO2↑+H2O,根据强酸制取弱酸的原理,硝酸的酸性强于碳酸,硝酸、碳酸分别为N、C的最高价含氧酸,所以可证明氮非金属性大于碳,C中为Na2SiO3溶液,二氧化碳通入反应生成硅酸沉淀,根据强酸制取弱酸的原理,碳酸的酸性强于硅酸,碳酸、硅酸分别为C、Si的最高价含氧酸,所以可证明碳的非金属性大于硅,C装置中观察到溶液变浑浊,
故答案为:CaCO3+2H+=Ca2++CO2↑+H2O;溶液变浑浊;
(2)硝酸易挥发,制取的二氧化碳中含有硝酸,若不除去硝酸,无法说明C装置中观察到溶液变浑浊是硝酸和硅酸盐反应,还是碳酸和硅酸盐反应,所以B装置是为了吸收挥发出的硝酸蒸气,
故答案为:除去二氧化碳中混有的硝酸蒸气;
(3)A中反应是碳酸钙和稀硝酸反应生成二氧化碳,C中为Na2SiO3溶液,二氧化碳通入反应生成硅酸沉淀,证明碳酸的酸性强于硅酸,所以碳酸、硝酸、硅酸的酸性强弱顺序是硝酸>碳酸>硅酸,根据实验现象和元素最高价含氧酸的酸性强弱判断元素非金属性强弱,酸性越强,非金属性越强,推知C、N、Si三种元素非金属性的强弱为N>C>Si,
故答案为:硝酸>碳酸>硅酸;N>C>Si.
实验Ⅱ:(4)A装置:浓盐酸与高锰酸钾反应生成氯气2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,氯气通入装置B:溴化钾溶液中,2Br-+Cl2═Br2+2Cl-;溶液出现红色,有溴单质生成,说明氯的非金属性强于溴,
故答案为:2Br-+Cl2═Br2+2Cl-;
(5)装置中挥发出来的溴或氯气都有毒,会污染空气,氢氧化钠能吸收溴单质、氯气,所以要用装置C:氢氧化钠溶液吸收,故答案为:吸收尾气;
(6)由2Br-+Cl2═Br2+2Cl-,则可以得出非金属性:Cl>Br,故答案为:Cl>Br.
点评 本题考查了实验设计和实验分析的判断,主要是非金属性强弱的判断依据,掌握物质性质和实验设计是解题关键,题目难度中等,注意把握比较金属性、非金属性的角度,把握实验方法.


 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:选择题
| A. | 可用灼烧的方法鉴别纯羊毛和合成纤维 | |
| B. | 没有水就没有生命 | |
| C. | 碳酸钡悬浊液可用作胃部X 射线透视的“钡餐” | |
| D. | 硅的导电性介于导体和绝缘体之间,晶体硅可用作半导体材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.01mol/L的氨水 | B. | 0.01mol/L的NaOH | ||
| C. | 0.01mol/L的CH3COOH | D. | 0.01mol/L的HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③⑤ | B. | ①②③ | C. | ②③④⑤ | D. | ①③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铅蓄电池充电时,阴极反应式为:PbSO4+2e-=Pb+SO42- | |
| B. | 用锌片做阳极,铁片做阴极,电解氯化锌溶液,铁片表面出现一层锌 | |
| C. | 钢柱在水下部分比在空气与水交界处更容易腐蚀 | |
| D. | 把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
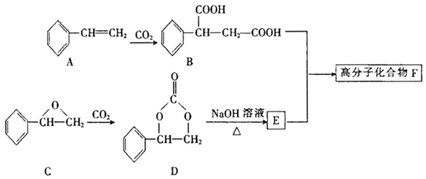
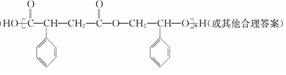
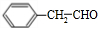 ,G与新制的Cu(OH)2悬浊液混合加热时发生反应的化学方程式为
,G与新制的Cu(OH)2悬浊液混合加热时发生反应的化学方程式为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com