
NA表示阿伏加德罗常数,下列叙述正确的是
A.1 L 1 mol·L-1的NaClO溶液中含有ClO-的数目为NA。
B.标准状况下,0.1 mol Cl2溶于水,转移电子的数目为0.1 NA。
C.2.3 g Na与O2完全反应生成3.6 g产物时失电子数是0.1×6.02×1023
D.标准状况下,11.2 L CH3CH2OH中含有的分子数为0.5NA
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源:2014-2015江苏省泰州市姜堰区高一上学期期末化学试卷(解析版) 题型:选择题
三氟化氮(NF3)是微电子工业中一种优良的等离子蚀刻气体。在潮湿的空气中能发生下列反应:3NF3+5H2O=2NO+HNO3+9HF。下列有关判断正确的是
A.反应中NF3是氧化剂,H2O是还原剂
B.反应中被氧化与被还原的原子物质的量之比为2∶1
C.若反应中生成0.2mol HNO3,则反应共转移0.4mol电子
D.NF3在潮湿空气中泄漏会产生红棕色气体
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省宿迁市高二下学期学业水平模拟化学试卷(解析版) 题型:选择题
化学与环境保护、社会可持续发展密切相关,下列做法合理的是
A.进口国外电子垃圾,回收其中的贵重金属
B.将地沟油回收加工为生物柴油,提高资源的利用率
C.大量生产超薄塑料袋,方便人们的日常生活
D.洗衣粉中添加三聚磷酸钠,增强去污的效果
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省菏泽市高三上学期期末考试化学B试卷(解析版) 题型:选择题
某稀硫酸和稀硝酸的混合溶液中c(SO42-)+c(NO3-)=2.5 molL-1.取200mL该混合酸,则能溶解铜的最大质量为
A.12.8g B.19.2g C.32.0g D.38.4g
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省菏泽市高三上学期期末考试化学B试卷(解析版) 题型:选择题
下列说法正确的是
A.c(H+)>c(OH-)的溶液一定显酸性
B.常温下,pH = 6 的溶液一定是酸溶液
C.电解稀硫酸或氢氧化钠溶液的产物不同
D.将纯水加热,其KW增大而pH不变
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省德州市高三2月期末统考化学试卷(解析版) 题型:填空题
(12分)【有机化学基础】
用甲苯生产一种常用的化妆品防霉剂,其生产过程如图(反应条件没有全部注明).

根据转化图填空
(1)有机物A的结构简式_____________
(2)在合成路线中,设计第③步反应的目的是:__________________________.
(3)写出反应⑤的化学方程式__________________________________________.
(4)请写出由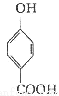 生成C7H5O3Na的化学反应方程式______________________________.
生成C7H5O3Na的化学反应方程式______________________________.
(5)下列有关说法正确的是_____________。

A.莽草酸、对羟基苯甲酸都属于芳香族化合物
b.1 mol莽草酸与NaOH溶液反应,最多消耗4 molNaOH
c.二者均可以发生酯化、氧化、加成等反应
d.利用FeCl3溶液可区别莽草酸和对羟基苯甲酸
(6)写出同时符合下列要求的 所有同分异构体的结构简式_____________.
所有同分异构体的结构简式_____________.
A.含苯环
b.可与FeCl3溶液发生显色反应
c.一氯代物有两种
d.能发生银镜反应,不能发生水解反应。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省德州市高三2月期末统考化学试卷(解析版) 题型:选择题
下列各组物质中,物质之间通过一步反应就能实现图示转化的是

A.①②③ B.①③④ C.①④ D.②④
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省泰州市姜堰区高三下学期期初联考化学试卷(解析版) 题型:简答题
(12分)锰的用途非常广泛,在钢铁工业中,锰的用量仅次于铁,90%的锰消耗于钢铁工业,10%的锰消耗于有色冶金、化工、电子、电池、农业等部门。以碳酸锰矿(主要成分为MnCO3,还含有铁、镍、钴等碳酸盐杂质)为原料生产金属锰的工艺流程如下:

已知25℃,部分物质的溶度积常数如下:
物质 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 | MnS | CoS | NiS |
Ksp | 2.1×10-13 | 3.0×10-16 | 5.0×10-16 | 1.0×10-11 | 5.0×10-22 | 1.0×10-22 |
(1)步骤Ⅰ中,MnCO3与硫酸反应的化学方程式是 。
(2)步骤Ⅰ中需要加入稍过量的硫酸,其目的有3点:①使矿物中的物质充分反应;②提供第Ⅱ步氧化时所需要的酸性环境;③ 。
(3)步骤Ⅱ中,MnO2在酸性条件下可将Fe2+氧化为Fe3+,该反应的离子方程式是 ,加氨水调节溶液的pH为5.0~6.0,以除去Fe3+。
(4)步骤Ⅲ中,滤渣2的主要成分是 。
(5)步骤Ⅳ中,在 (填“阴”或“阳”)极析出Mn,电极反应方程式为 。
(6)电解后的废水中还含有Mn2+,常用石灰乳进行一级沉降得到Mn(OH)2沉淀,过滤后再向滤液中加入适量Na2S,进行二级沉降。欲使溶液中c(Mn2+)≤1.0×10-5 mol·L-1,则应保持溶液中c(S2-)≥ mol·L-1。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省八市高三年级三月联考理综化学试卷(解析版) 题型:推断题
选考【化学——选修5:有机化学基础】(15分)
烃A的质谱图中,质荷比最大的数值为42。碳氢两元素的质量比为6:1,其核磁共振氢谱有三个峰,峰的面积比为1:2:3。A与其他有机物之间的关系如下图所示:

已知:CH2=CH2 HOCH2CH2OH,回答下列问题:
HOCH2CH2OH,回答下列问题:
(1)F的结构简式为 。
(2)有机物C中的官能团名称 。
(3)指出下列转化的化学反应类型:A→B E→G 。
(4)写出C与新制的氢氧化铜反应的化学方程式 。
(5)E在一定条件下可以相互反应生成一种六元环有机物,则此反应的化学方程式为 。
(6)与E互为同分异构体,且属于酯类的有机物,除CH3OCOOCH3、CH3CH2OCOOH外还有 种(分子中无O—O键)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com