
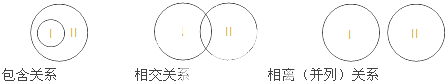
| 概念I | 概念II | 相互关系 | |
| A | 共价分子 | 共价化合物 | 包含关系 |
| B | 分解反应 | 吸热反应 | 包含关系 |
| C | 非金属氧化物 | 酸性氧化物 | 相交关系 |
| D | 离子互换反应 | 氧化还原反应 | 相离(并列)关系 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、共价分子包括单质和化合物;
B、分解反应是不一定都是吸热的,而且分解反应只是吸热反应中的一种;
C、大多数的非金属氧化物是酸性氧化物,但酸性氧化物不一定是非金属氧化物;
D、离子互换反应即复分解反应,一定无电子的得失,故一定不是氧化还原反应.
解答 解:A、共价分子包括单质和化合物,但是共价化合物是化合物的范畴,二者不是包含关系,故A错误;
B、绝大多数的分解反应是吸热的,但分解反应是不一定都是吸热的;吸热反应也不一定是分解反应,故两者为相交关系,故B错误;
C、非金属氧化物不一定是酸性氧化物,如H2、CO,酸性氧化物也不一定是非金属氧化物,如Mn2O7,故两者的关系为相交关系,故C正确;
D、离子互换反应一定不是氧化还原反应,氧化还原反应一定不是离子互换反应,故两者是相离(并列)关系,故D正确;
故选CD.
点评 物质的分类是重点的基础化学知识,但却是学习难点之一,要能正确地、合理地对物质作出正确分类,首先要理解物质分类的有关概念,抓住概念间的相互关系和本质区别.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO3的物质的量为4.5mol的状态为平衡状态 | |
| B. | O2的平均反应速率为0.4amol•(L•min)-1 | |
| C. | SO2和O2的反应百分率相等 | |
| D. | 达到化学平衡状态时容器内压强减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,Na2O2中的化学键类型有离子键和非极性共价键;
,Na2O2中的化学键类型有离子键和非极性共价键;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
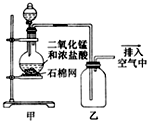
| A. | 该装置图中至少存在两处明显错误 | |
| B. | 烧瓶中的MnO2可换成KMnO4 | |
| C. | 在乙后连一盛有饱和食盐水的烧杯可进行尾气处理 | |
| D. | 在集气瓶的导管口处放一片湿润的淀粉碘化钾试纸可以证明是否有氯气逸出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 当n=1时,X可能是C | B. | 当n=1时,X可能是Al | ||
| C. | 当n=2时,X可能是S | D. | 当n=2时,X可能是Na |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(SO32-)=0.5 mol•L-1的溶液中:ClO-、Na+、Cl-、CO32- | |
| B. | pH=1的溶液中:NH4+、Na+、SO42-、Fe3+ | |
| C. | 强碱性溶液中:Na+、AlO2-、NO3-、HCO3- | |
| D. | 水电离产生的c(H+)=1×10-14mol•L-1的溶液中:HCO3-、NH4+、Cl-、Ca2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将少量某物质的溶液滴加到新制氢氧化铜中,加热 | 有红色沉淀生成 | 该物质一定属于醛类 |
| B | 向AgNO3溶液中滴加过量氨水 | 溶液澄清 | Ag+与NH3•H2O能大量共存 |
| C | 将某气体通入品红溶液中 | 品红溶液褪色 | 该气体一定是SO2 |
| D | 将0.1mol/L MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol/L CuSO4溶液 | 先有白色沉淀生成后变为浅蓝色沉淀 | Cu(OH)2的溶解度小于Mg(OH)2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com