
 根据下图所示,推断物质X的化学式,并选择适宜的物质完成图中各步转化,写出相应的化学方程式.
根据下图所示,推断物质X的化学式,并选择适宜的物质完成图中各步转化,写出相应的化学方程式.

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:江苏省盐城中学2008-2009学年度高二上学期期中考试(化学)(选修) 题型:022
氢叠氮酸HN3是一种弱酸,它和CH3COOH相似为一元弱酸,N3-被称为类卤离子,试回答下列问题:
(1)HN3呈弱酸性的电离方程式为:_____________
(2)若HN3分子中每个原子均达到了8电子或2电子稳定结构,写出HN3的电子式:_____________
(3)实际情况并不是(2)中所述,HN3的分子成键情况如下图所示,

则HN3分子中有________个σ键,其中与H相连的N原子的杂化类型为________
(4)![]() 与常见分子________互为等电子体,则推断
与常见分子________互为等电子体,则推断![]() 的空间构型是________.
的空间构型是________.
(5)以金属Cu、石墨作电极,以盐酸、HN3混合溶液作电解质溶液组成原电池,正极有气泡产生;一段时间后电流减弱,在负极周围滴入几滴浓盐酸后又使电流增大,已知原电池总反应为:2HCl+2Cu=2CuCl+H2↑,CuCl微溶于水,易溶于浓盐酸.
写出正极反应式_____________,负极反应式_____________,根据已学的分子结构知识推断CuCl溶于浓盐酸的可能原因是生成了_________物.
查看答案和解析>>
科目:高中化学 来源:河北省冀州中学2012届高三上学期期中考试化学试题(B) 题型:022
(Ⅰ)有一无色溶液,其中可能含有Fe3+、Al3+、Fe2+、Mg2+、Cu2+、NH4+、K+、CO32-、SO42-等离子的几种,取此溶液分别进行了四个实验,其操作和有关现象如下图所示:

请根据上图推断:
(1)原溶液中一定存在的离子有________.
(2)写出实验④中沉淀量由A→B过程中所发生反应的离子方程式:________.
(3)实验③中产生无色无味气体所发生的化学方程式为:________.
(Ⅱ)已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去.现有一个氧化还原反应的体系中共有KCl、Cl2、H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质:
(4)该反应中,化合价升高的反应物是________.
(5)写出一个包含上述七种物质的氧化还原反应方程式:________.
(6)上述反应中,1 mol氧化剂在反应中得到电子的数目为________.
(7)下图:将浓盐酸滴入高锰酸钾固体中,制取适量黄绿色气体的简易装置,请回答装置B、C、D的作用分别是:
B________;C________;D________.
查看答案和解析>>
科目:高中化学 来源:河北省冀州中学2012届高三上学期期中考试化学试题(A) 题型:022
(Ⅰ)有一无色溶液,其中可能含有Fe3+、Al3+、Fe2+、Mg2+、Cu2+、NH4+、K+、CO32-、SO42-等离子的几种,取此溶液分别进行了四个实验,其操作和有关现象如下图所示:
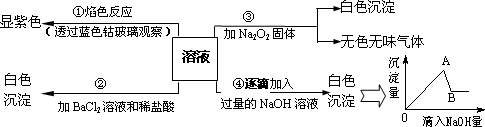
请根据上图推断:
(1)原溶液中一定存在的离子有________.
(2)写出实验④中沉淀量由A→B过程中所发生反应的离子方程式:________.
(3)实验③中产生无色无味气体所发生的化学方程式为:________.
(Ⅱ)已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去.现有一个氧化还原反应的体系中共有KCl、Cl2、H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质:
(4)该反应中,化合价升高的反应物是________.
(5)写出一个包含上述七种物质的氧化还原反应方程式:________.
(6)上述反应中,1 mol氧化剂在反应中得到电子的数目为________.
(7)下图:将浓盐酸滴入高锰酸钾固体中,制取适量黄绿色气体的简易装置,请回答装置B、C、D的作用分别是:
B________;C________;D________.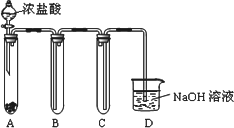
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com