
| A�� | 11.7g | B�� | 23.4 g | C�� | 35.1g | D�� | 58.5 |
���� ����������200mL��2mol/L��ϡ�����з���ǡ����ȫ��Ӧ������ȫ�ų�������̼���壬��Ӧ����Һ������ΪNaCl�������ԭ���غ���㣮
��� �⣺����������200mL��2mol/L��ϡ�����з���ǡ����ȫ��Ӧ������ȫ�ų�������̼���壬��Ӧ����Һ������ΪNaCl������ԭ���غ��֪��n��NaCl��=n��HCl��=0.2L��2mol/L=0.4mol��
�������ᷴӦ�����Һ���ɡ����ճ�����������Ϊ0.4mol��58.5g/mol=23.4 g��
��ѡB��
���� ���⿼�黯ѧ��Ӧ�ļ��㣬Ϊ��Ƶ���㣬���շ�Ӧ����ԭ���غ�Ϊ���Ĺؼ������ط�������������Ŀ��飬ע���غ㷨��Ӧ�ã���Ŀ�ѶȲ���


 ϰ�⾫ѡϵ�д�
ϰ�⾫ѡϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Al����ijǿ��ʧȥ2mol���ӣ�һ������2gH2 | |
| B�� | 0.1mol�£�N2H4���й��õ��ӶԽ�ĿΪ0.5NA | |
| C�� | 64.0gSO2������O2����SO3����ת�ƽ�Ϊ2NA | |
| D�� | 2L0.5mol/L�������Һ�����ӵ����Ϊ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 2��2-����������2��4-���������һ�ȴ�����������ͬ | |
| B�� | ���顢�����ѻ�������Һ������ʹ���Ը��������Һ��ɫ | |
| C�� | Na��Cl2��ȼ�յ������ﺬ���Ӽ�������NaCl����ɵ��� | |
| D�� | �Ҵ��ķе������ķе�ͣ������Ҵ��������ͨ������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ܽ�������ʱ��й� | |
| B�� | �¶ȡ�ѹǿһ��ʱ�����ȵ������ӷ�Ӧ��һ�����Է����� | |
| C�� | ��Ӧ�ʱ��Ǿ�����Ӧ�ܷ��Է����е�Ψһ���� | |
| D�� | ���¶ȡ�ѹǿһ���������£������غ������ع�ͬ����һ����ѧ��Ӧ�ķ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ƕ�����̼������̼ԭ�����ĸ��۵��ӣ�̼ԭ�Ӽ��Լ�̼������ԭ�Ӽ�ṹ���� | |
| B�� | ���Ƿ�Ӧ�ܸ��� | |
| C�� | ��ȡ���ǵķ����ܶ� | |
| D�� | ���Ƕ��Ƿǵ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
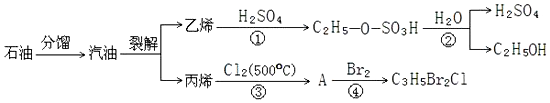
| A�� | ʯ�ͷ�����ѽ�����ڻ�ѧ�仯 | |
| B�� | ��Ӧ�٢ڱ��������������ϩˮ�������Ҵ��Ĵ��� | |
| C�� | ��Ӧ���뷴Ӧ�ܾ����ڼӳɷ�Ӧ | |
| D�� | ��Ӧ�۵�ԭ��������Ϊ100% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ӧ�ٵ�ƽ�ⳣ��K1=$\frac{c��C{O}_{2}��•c��Cu��}{c��CO��•c��CuO��}$ | |
| B�� | ��Ӧ�۵�ƽ�ⳣ��K=$\frac{{K}_{1}}{{K}_{2}}$ | |
| C�� | ���ڷ�Ӧ�ۣ�����ʱ�����¶����ߣ�H2��Ũ�ȼ�С����÷�Ӧ���ʱ�Ϊ��ֵ | |
| D�� | ���ڷ�Ӧ�ڣ����º���ʱ��������CuO��ƽ���������ƶ���H2��Ũ�ȼ�С |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com