
| A. | 硫元素的质量比为5:4 | B. | 任何情况下体积比均为1:1 | ||
| C. | 含有的O2、O3两分子数之比为1:1 | D. | SO2、SO3两分子数之比为1:1 |
分析 A.相同物质的量的SO2和SO3含有相同的S原子,则S元素的质量相等;
B.不同条件下气体摩尔体积不一定相等,则二者的体积不一定相等;
C.二氧化硫和三氧化硫分子中不存在O2、O3分子.
D.根据N=nNA可知二者分子数之比为1:1.
解答 解:A.相同物质的量的SO2和SO3分子中含有S的物质的量相等,根据m=nM可知二者含有硫元素的质量相等,含有硫元素的质量比为1:1,故A错误;
B.在不同条件下气体摩尔体积不一定相等,则二者占有的体积不一定相等,故B错误;
C.SO2和SO3分子中不存在O2、O3分子,故C错误;
D.根据N=nNA可知,相同物质的量的SO2、SO3含有分子数之比为1:1,故D正确;
故选D.
点评 本题考查了物质的量的计算,题目难度不大,明确气体摩尔体积的使用条件为解答关键,注意掌握物质的量与摩尔质量、阿伏伽德罗常数、气体摩尔体积之间的关系,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 月波成露露成霜,借与南枝作淡妆 | B. | 春蚕到死丝方尽,蜡炬成灰泪始干 | ||
| C. | 粉骨碎身浑不怕,要留清白在人间 | D. | 莫道雪融便无迹,雪融成水水成冰 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液 | |
| B. | 将氧气和氢气的混合气体通过灼热的氧化铜,以除去其中的氢气 | |
| C. | 用溶解、过滤的方法分离K2MnO4和MnO2固体的混合物 | |
| D. | 用分液的方法分离煤油和汽油 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
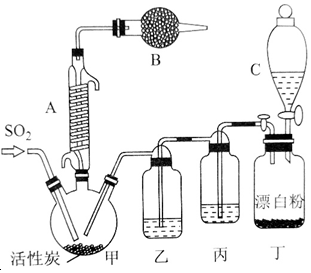 有关信息如下:硫酰氯通常条件下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中“发烟”;100℃以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解.回答下列问题:
有关信息如下:硫酰氯通常条件下为无色液体,熔点为-54.1℃,沸点为69.1℃,在潮湿空气中“发烟”;100℃以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
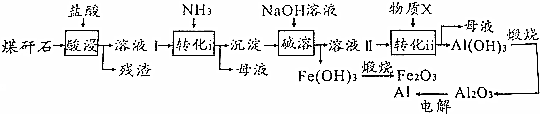
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com