
 下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )| a | b | c | |
| A | Al | AlCl3 | Al(OH)3 |
| B | HNO3 | NO | NO2 |
| C | Si | SiO2 | H2SiO3 |
| D | Na2O | Na2CO3 | NaHCO3 |
| A、A | B、B | C、C | D、D |


科目:高中化学 来源: 题型:
 利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实.某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如下:
利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实.某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如下:查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
| Y | CO2 | Fe2O3 | SiO2 | FeCl3 |
| W | MgO | Al2O3 | CO2 | CuCl2 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾[KAl(SO4)2?12H2O]在水中能形成Al(OH)3胶体,可用作净水剂 |
| B、用蒸馏水充分浸润燃尽后的火柴头,然后加入硝酸银和稀硝酸检验火柴头中氯元素 |
| C、浓H2SO4有强氧化性,常温下能与Cu发生剧烈反应 |
| D、用食醋和碘化钾淀粉试纸可以鉴别NaNO2和NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由分子构成的物质中一定含有共价键 |
| B、形成共价键的元素中不一定全是非金属元素 |
| C、两种粒子,若核外电子排布完全相同,则其化学性质相同 |
| D、不同的原子的化学性质可能相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Wn+、Xm+、Ym-、Zn-的离子半径依次增大 |
| B、Y、Z的气态氢化物的热稳定性:YHm>HnZ |
| C、W、X、Y、Z的最高价氧化物对应的水化物都是强电解质 |
| D、W、X、Y、Z的最高价氧化物对应的水化物的碱性依次减弱,酸性依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
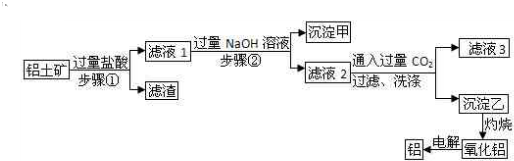
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com