
【题目】焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一.某研究小组进行如下实验:采用如图1装置(实验前已除尽装置内的空气)制取Na2S2O5 . 已知:①装置Ⅱ中有Na2S2O5晶体析出,发生的反应为Na2SO3+SO2═Na2S2O5 .
②Na2S2O5晶体在空气中被氧化生成Na2SO4 . 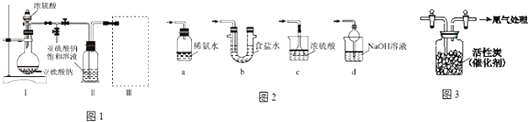
(1)装置Ⅰ中产生气体的化学方程式为 .
(2)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是 .
(3)装置Ⅲ用于处理尾气,可选用的最合理装置(图2)(夹持仪器已略去)为(填序号).
(4)检测Na2S2O5晶体在空气中已被氧化的实验方案是 .
(5)为了研究干燥的Cl2与干燥SO2反应及进行程度.用如图3所示装置收集满干燥的Cl2 , 再通入干燥SO2 , 集气瓶中立即产生无色液体SO2Cl2 , 充分反应后,将液体和剩余气体分离.继续用NaOH溶液吸收分离出的气体,用足量稀盐酸酸化后,再滴加BaCl2溶液,产生白色沉淀,该白色沉淀是 , 由此可知反应后剩余气必然存在气体,综合实验信息,请写出干燥的SO2与Cl2反应的化学方程式 .
【答案】
(1)Na2SO3+H2SO4═Na2SO4+SO2↑+H2O
(2)过滤
(3)d
(4)取少量Na2S2O5晶体于试管中,加适量水溶解,滴加足量盐酸,振荡,再滴入氯化钡溶液,有白色沉淀生成
(5)白色沉淀是BaSO4;混合气体中必然存在SO2和Cl2两种气体;SO2+Cl2 ![]() SO2Cl2
SO2Cl2
【解析】解:(1)由装置Ⅱ中发生的反应可知,装置Ⅰ中产生的气体为SO2 , 亚硫酸钠与硫酸反应生成硫酸钠、二氧化硫与水,反应方程式为:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O,所以答案是:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O;(2)装置Ⅱ中获得已析出的晶体,分离固体与液态,应采取过滤进行分离,
所以答案是:过滤;(3)a.装置应将导管深入氨水中可以吸收二氧化硫,但为密闭环境,装置内压强增大易产生安全事故,故错误;
b.该装置吸收二氧化硫能力较差,且为密闭环境,装置内压强增大易产生安全事故,故错误;
c.该装置不能吸收二氧化硫,所以无法实现实验目的,故错误;
d.该装置中氢氧化钠与二氧化硫反应,可以吸收,且防止倒吸,故正确;
所以答案是:d;(4)Na2S2O5中S元素的化合价为+4价,因此会被氧化为为+6价,即晶体在空气中易被氧化为Na2SO4 , 用盐酸、氯化钡溶液检验样品中是否含有硫酸根即可,实验方案为:取少量Na2S2O5晶体于试管中,加入适量水溶解,滴加盐酸,振荡,再滴加氯化钡溶液,有白色沉淀生成,
所以答案是:取少量Na2S2O5晶体于试管中,加入适量水溶解,滴加盐酸,振荡,再滴加氯化钡溶液,有白色沉淀生成;(5)生成的白色沉淀为BaSO4 , 说明NaOH溶液吸收分离出的气体成分不是单一的SO2或Cl2,而是二者的混合气体,在水溶液里发生了氧化还原反应,生成了硫酸根离子,同时也可知SO2与Cl2生成SO2Cl2的反应是可逆反应,因为反应物的转化率没有达到100%,所以答案是:白色沉淀是BaSO4;混合气体中必然存在SO2和Cl2两种气体;SO2+Cl2 ![]() SO2Cl2 .
SO2Cl2 .


科目:高中化学 来源: 题型:
【题目】常温下,将除去表面氧化膜的A1、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示。反应过程中有红棕色气体产生。下列说法错误的是 ( )

A. t1时刻前,A1片的电极反应为:2A1+3H2O - 6e- ═ A12O3+6H+
B. t1时,因A1在浓硝酸中钝化,氧化膜阻碍了A1继续反应
C. t1之后,负极Cu失电子,电流方向发生改变
D. 烧杯中发生的离子反应为:2NO2+2OH- ═ 2NO3-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酶指具有生物催化功能的高分子物质.在酶的催化反应体系中,反应物分子被称为底物,底物通过酶的催化转化为其他分子.几乎所有的细胞活动进程都需要酶的参与,以提高效率.请回答下列问题:
(1)酶氧化酶与酚类底物在细胞中能实现分类存放,是因为细胞内具有 系统,组成该系统的结构具有的功能特性是 .茶叶细胞中也存在众多种类的酚类物质与酚氧化酶.绿茶制取过程中必须先进行热锅高温炒制,这一过程的目的是 .
(2)茶树的Rubicon酶在CO2浓度较高时,该酶催化C2与CO2反应,Rubicon酶的存在场所为 ;该酶具有“两面性”,在O2浓度较高时,该酶催化C2与O2反应,产物经一系列变化后到线粒体中会产生CO2,其“两面性”与酶的 (特性)相矛盾.
(3)如图中曲线表示将酶在不同温度下保温足够长时间,再在酶活性最高的温度下测其残余酶活性,由图可得出: .为了验证这一结论,请以耐高温的纤维素分解酶为实验材料,比较在低温和最适温度下储存对酶活性的影响,写出实验设计思路: .

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示(气体体积均在相同状况下测定)。欲使溶液恢复到起始状态,可向溶液中加入
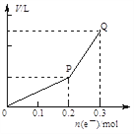
A. 0.1 mol CuO B. 0.05 mol Cu2(OH)2CO3
C. 0.1 mol Cu(OH)2 D. 0.1 mol CuCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁晶体(FeSO47H2O)在医药上作补血剂.某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质.实验步骤如下: 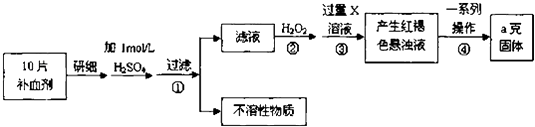
请回答下列问题:
(1)步骤①滤液中滴加KSCN溶液后滤液变为红色,则该溶液中含有(填离子符号),检验滤液中还存在Fe2+的方法为(注明试剂、现象).
(2)步骤②加入过量H2O2的目的是 .
(3)步骤③中反应的离子方程式为
(4)步骤④中一系列处理的操作步骤包括:过滤、、灼烧、、称量.
(5)若实验无损耗,则每片补血剂含铁元素的质量为g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于食品添加剂,人们有不少误解,甚至是“谈虎色变”.根据国家的相关规定,食品按要求添加食品添加剂是安全的,只有过度使用或使用不安全的添加剂才会对人体造成伤害.下列物质是我们生活中常见的添加剂,请对它们进行分类:
①柠檬黄②加铁酱油中的铁③味精④苯甲酸钠
(1)着色剂:(填序号,下同);
(2)调味剂:;
(3)防腐剂:;
(4)营养强化剂: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一在空气中放置了一段时间的NaOH固体,经分析测知其含水7%,含Na2CO353%,其余为NaOH。取10克该样品恰好和100毫升2molL-1的盐酸反应,蒸发反应后的溶液可得到固体的质量为( )
A.5.85克B.10克C.17.55克D.11.7克
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com