
36��5 g HCl�ܽ���1 Lˮ�У�ˮ���ܶȽ���Ϊl g��cm3����������Һ���ܶ�Ϊ��g��cm3����������Ϊ�أ����ʵ���Ũ��Ϊc mol��L��NA��ʾ�����ӵ���������������������ȷ����
Lˮ�У�ˮ���ܶȽ���Ϊl g��cm3����������Һ���ܶ�Ϊ��g��cm3����������Ϊ�أ����ʵ���Ũ��Ϊc mol��L��NA��ʾ�����ӵ���������������������ȷ����
A��������Һ�����ʵ���Ũ�ȣ�c��1 mol��L��
B��������Һ�к���NA��HCl����
C��36��5 g HCl����ռ�е����Ϊ22��4 L
D��������Һ�������������أ�36��5 c��1000P

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ȳ��Ϊԭ�Ͽɺϳ��л���H2MA������һ���ϳɸ߷��ӻ�����PMLA��
I������Ȳ�Ⱥϳ���C��

��֪��

��1��A�����еĹ�����������_______��_______��
��2��A��һ��ͬ���칹����������������ṹ��ʽ��________________
��3��Bת��ΪC�Ļ�ѧ����ʽ��________________________________________���䷴Ӧ������_______��
II������C�ϳ�PMLA��·�����¡�

��֪��

��4��1 mol�л���H������NaHCO3��Һ��Ӧ���ɱ�״���µ�CO2 44.8 L��H��˳���칹���䷴ʽ�ṹ��ʽ��________________
��5��E�Ľṹ��ʽ��________________
��6��G��NaOH��Һ�ڼ��������·�Ӧ�Ļ�ѧ����ʽ��_________________________
��7������PMLA�ж��ֽṹ��д����H2MA��PMLA�Ļ�ѧ����ʽ����дһ�֣�________________________________________________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ݱ�����Ϣ�жϣ�����ѡ������ȷ����
| ��� | ��Ӧ�� | ���� |
| �� | KMnO4 ��H2O2 ��H2SO4 | K2SO4 ��MnSO4 ������������ |
| �� | Cl2 ��FeBr2 | FeCl3 ��FeBr3 |
| �� | MnO4�� �������� | Cl2 ��Mn2+ ������������ |
A���ڢ��鷴Ӧ���������ΪH2O�� O2
B���ڢ��鷴Ӧ��Cl2 �� FeBr2�����ʵ���֮��С�ڻ����1�U2
C���ڢ��鷴Ӧ������1mol Cl2��ת�Ƶ���2mol
D����������ǿ����˳��ΪMnO4- > Cl2 > Fe3+ > Br2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и���Ӧ��Ӧ�����ӷ���ʽ��ȷ���ǣ� ��
A������������Һ��ͨ�������������ClO�� + H2O + SO2 = HClO + HSO3��
B����̼��������Һ�м����������������Һ2HCO3���� Ca2����2OH��= CaCO3����2H2O��CO32��
C������������Һ��������Һ��Ӧ�õ�������ҺBa2����OH���� H����SO42�� = BaSO4����H2O
D��50 mL 1mol/L��NaOH��Һ��ͨ��0.03 mol H2S 5OH�� + 3H2S = HS�� + 2S2�� + 5H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���̫������� �û���������ۻ����ϣ���Ħ������Ϊ140 g��mol��1�����й�Ԫ�ص���������Ϊ60%����֪1 molNH3�������Ļ������ҳ�ַ�Ӧ��ɵõ�35 g ����6 g H2����ҵ�����ҵ��������£�
�û���������ۻ����ϣ���Ħ������Ϊ140 g��mol��1�����й�Ԫ�ص���������Ϊ60%����֪1 molNH3�������Ļ������ҳ�ַ�Ӧ��ɵõ�35 g ����6 g H2����ҵ�����ҵ��������£�
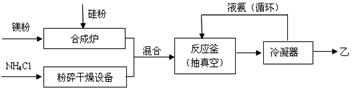
��ش��������⣺
��1���ҵĵ���ʽ�� ���Ƚ����ȶ��ԣ���_______NH3�����������
��2��NH3�������Ļ������ҷ�Ӧ�ƼĻ�ѧ����ʽ�� ��
��3���ϳ�¯���������ڱ��������¸��ºϳɣ���������������������� ������ĸ��ţ���
A��O2 B��H2 C��N2 D��CO2 E��Ar
��4�����������ҵĹ�����Һ����������______________________________________��
��5����������H2SO4��Һ��Ӧֻ�õ�H2SiO3����M���ֲ��д���÷�Ӧ�����ӷ���ʽ ���������֤������M��ʵ�鷽�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
1 Lij�����Һ�п��ܺ��е��������±�:
| ���ܴ������е������� | H+ NH4+ Al3+ K+ |
| ���ܴ������е������� | Cl- Br- I‑ ClO‑ AlO2- |
��1��������Һ����μ���NaOH��Һ���ʵ����ȣ����� ��������������ʵ�����n�������NaOH��Һ�������v���Ĺ�ϵ��ͼ��ʾ��
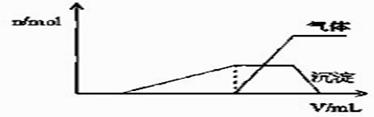
�������Һ��ȷ�����е������� ; �ڲ���ȷ���Ƿ��е��������� , ��Ҫȷ������ڿɲ�������ʵ���� ; �ܿ϶������ڵ��������� ��
(2)�����,����Һ�к��д�����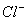 ��
��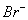 ��
��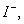 ����1 L�û����Һ��ͨ��һ������
����1 L�û����Һ��ͨ��һ������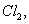 ��Һ��
��Һ��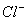 ��
��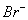 ��
��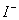 �����ʵ�����ͨ��
�����ʵ�����ͨ��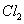 �����(��״��)�Ĺ�ϵ���±���ʾ,������ش���������:
�����(��״��)�Ĺ�ϵ���±���ʾ,������ش���������:
| Cl2����� ����״���� | 2.8 L | 5.6L | 11.2L |
| n��Cl-�� | 1.25mol | 1.5mol | 2mol |
| n��Br-�� | 1.5mol | 1.4mol | 0.9mol |
| n��I-�� | a mol | 0 | 0 |
�ٵ�ͨ��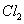 �����Ϊ2.8 Lʱ,��Һ�з�����Ӧ�����ӷ���ʽΪ �� ��ԭ��Һ��
�����Ϊ2.8 Lʱ,��Һ�з�����Ӧ�����ӷ���ʽΪ �� ��ԭ��Һ��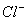 ��
��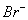 ��
��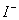 �����ʵ���Ũ��֮��Ϊ ��
�����ʵ���Ũ��֮��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij��Һ�к���HCO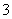 ��CO
��CO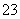 ��SO
��SO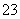 ��Na����NO
��Na����NO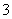 �������ӡ��������м���Na2O2��ĩ��ַ�Ӧ����Һ����仯���Բ��ƣ���
�������ӡ��������м���Na2O2��ĩ��ַ�Ӧ����Һ����仯���Բ��ƣ��� ��Һ������Ũ�ȱ��ֲ������
��Һ������Ũ�ȱ��ֲ������
A��NO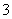 B��CO
B��CO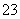 ��NO
��NO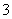
C��SO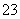 ��NO
��NO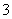 D��CO
D��CO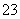 ��NO
��NO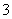 ��Na��
��Na��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
һ���¶��£�1 mol X��n mol Y�����Ϊ2 L���ܱ������з������·�Ӧ��X(g)��Y(g)  2Z(g)��M(s),5 min��ﵽƽ�⣬��ʱ����2a mol Z������˵����ȷ���� (����)��
2Z(g)��M(s),5 min��ﵽƽ�⣬��ʱ����2a mol Z������˵����ȷ���� (����)��
A����X��ʾ�˷�Ӧ�ķ�Ӧ������(0.1��2a) mol·L��1·min��1
B�������������������ٷ����仯ʱ��˵����Ӧ�ﵽƽ��״̬
C����ƽ������ϵ�м���1 mol M��ƽ�����淴Ӧ�����ƶ�
D��������ƽ����ϵ���ٳ���1 mol X��v������v����С��ƽ�������ƶ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com