
��֪��Ӧ2CH3OH(g) CH3OCH3(g)��H2O(g)ij�¶��µ�ƽ�ⳣ��Ϊ400�����¶��£���2 L���ܱ������м���a mol CH3OH����Ӧ��ijʱ�̲�ø���ֵ�Ũ�����£�
CH3OCH3(g)��H2O(g)ij�¶��µ�ƽ�ⳣ��Ϊ400�����¶��£���2 L���ܱ������м���a mol CH3OH����Ӧ��ijʱ�̲�ø���ֵ�Ũ�����£�
���� | CH3OH | CH3OCH3 | H2O |
Ũ��/(mol��L��1) | 0.44 | 0.6 | 0.6 |
����˵����ȷ����
A��a = 1.64
B����ʱ������Ӧ���ʴ����淴Ӧ����
C������ʼʱ����2a mol CH3OH����ﵽƽ��ʱCH3OH��ת��������
D������������ƽ��Ħ���������ٱ仯����˵����Ӧ�Ѵﵽƽ��״̬

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ɹŸ�һ���¿�һ��ѧ���������棩 ���ͣ�ʵ����
��1�����ʵ������98����Ũ���ᣨ�ܶ�Ϊ1.8g��cm-3�� ����2.4 mol��L-1��ϡ����250mL����������Ũ��������Ϊ________mL����ʵ��ʱӦ�� ��ȡŨ���ᡣ
��2�����Ʋ����ɷֽ�����¼�����������ȷ�IJ���˳����___________________
A��������ƿ��ע����������ˮ������Ƿ�©ˮ
B������������ˮϴ���ձ���������������Һע������ƿ�����ظ���������
C��������ȴ��ϡ����ע���Ѽ�鲻©ˮ������ƿ��
D�����ݼ��㣬����Ͳ��ȡһ�������Ũ����
E.��Ũ�������ձ�������ע��ʢ������ˮ��С�ձ��У��������ò���������
F.��������ƿ���ӣ���ҡ��
G.�ý�ͷ�ιܵμ�����ˮ��ʹ��Һ����ǡ����̶�����
H.����������ƿ��С�ĵؼ�����ˮ��ʹҺ��ӽ��̶���1~2 cm
��3�����ڴ������, ʹ�õ���Ũ�����ݱ���ȷ��ƫ�����______________��
A��ʹ������ƿ������Һʱ, ����Һ�涨�ݺ�������Һ��Ũ��
B��û��������ˮϴ�ձ�2-3�Σ�����ϴҺ��������ƿ��
C������ƿ������ˮϴ����û�к��
D������ʱ���μ�����ˮ����ʹҺ���Ը��ڿ̶��ߣ�����������ˮʹҺ�氼����̶�������
E.����õ���Һ����������ˮϴ����ĩ�ɵ��Լ�ƿ�б���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�츣��ʡ��������У������ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ʵ����
��ҵ����ij��������Ҫ�ɷ���Cu2O������������Al2O3��Fe2O3��SiO2����ȡͭ�IJ����������£�
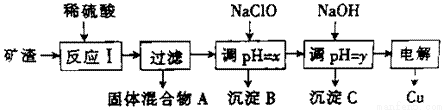
��֪����Cu2O+2H+��Cu+Cu2++H2O ��ijЩ�����������↑ʼ���������ȫ����ʱ��pH
������ |
|
|
|
|
��ʼ����pH | 5.4 | 4.0 | 2.2 | 5.8 |
�������pH | 6.7 | 5.2 | 3.2 | 8.8 |
��1����ӦI�У�����Ԫ���йط�Ӧ�����ӷ���ʽΪ �� ��
��2��y����ֵ��Χ�� ��
��3�����ϲ����е�NaOH������__________���棨����ĸ��
A��CuO B��NH4Cl C��Cu��OH��2
��4���������У������������Ϊ_____________________��
��5����NaClO��pH�����ɳ���B��ͬʱ����һ�־���Ư�����õ����ʣ��Ҹ������뻹ԭ��������ʵ���֮��Ϊ4:1,�÷�Ӧ�����ӷ���ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�츣��ʡ��������У������ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵������ȷ���ǣ� ��
A���ɱ���Һ̬�Ȼ��ⶼ�ǵ����
B�������Ƿ���ж����ЧӦ������ɢϵ��Ϊ��Һ����Һ�ͽ���
C�� NaOH�����мȺ������Ӽ��ֺ��й��ۼ�
D��Na2O��Fe2O3�� Al2O3�����ڼ�����������������ӻ�����
Al2O3�����ڼ�����������������ӻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�챱���и�����ѧ�����л�ѧ�Ծ��������棩 ���ͣ������
��������Ũ�Ⱦ�Ϊ0.1 mol/L�ĵ������Һ��
��Na2CO3���� NaHCO3���� ����CH3COONH4���� NH4HCO3
����CH3COONH4���� NH4HCO3
��1������5�����ʵ���Һ�����������������ռ���Һ��Ӧ���ǣ���д��ţ� ��
��2����֪��Һ�ܳ����ԣ�����Һ������Ũ���ɴ�С��˳���� ��
��3����֪��Һ�ݳʼ��ԣ��ȽϢܡ�������Һ������ԣ����Եó��Ľ����� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�챱���и�����ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ˮ�ۺ�����Ҫ���Ͽɳ�����չ��ԭ�������Ϲ�ҵ��ϵ�����֣���ͼ��ʾ��

����˵������ȷ����
A�����пɲ�������
B�����п�ͨ����ⱥ���Ȼ�þ��Һ�ƽ���þ
C�����������漰��������ԭ��Ӧ
D���ܵIJ�Ʒ���������ᡢƯ��Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�챱���и�����ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧ���ճ����������ء�����˵���У�����ȷ����
A����ȩ����ʳƷ������ B������������������ҩ
C���Ȼ��ƿ���ʳƷ��ζ�� D����ʯ�ҿ���ʳƷ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���㽭ʡ�����и�һ10���¿���ѧ���������棩 ���ͣ�ѡ����
���и������� ��ǰ�����ڵ���ʣ��������ڷǵ���ʵ��ǣ� ��
��ǰ�����ڵ���ʣ��������ڷǵ���ʵ��ǣ� ��
A��MgCl2���塢ʳ����Һ B��Na 2O���ɱ�
2O���ɱ�
C�����ڵ�KOH��Һ̬�� D�����ᡢ��ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���Ĵ�ʡ�߶�10���¿���ѧ���������棩 ���ͣ�ѡ����
����˵������ȷ���ǣ� ��
A��10 L 0.05mol��L��1Ba��OH��2��Һ��10 L 0.05mol��L��1 H2SO4��Ӧʱ�ķ�Ӧ�����к���
B����2H2��g��+O2��g��=2H2O��l�� ��H =-571.6 kJ��mol-1֪���÷�Ӧ�ķ�Ӧ��Ϊ571.6 kJ��mol-1
C����2H2��l��+O2��l��=2H2O��g�� ��H =-482.6 kJ��mol-1֪��H2��ȼ����Ϊ482.6 kJ��mol-1
D����C3H8��g��+5O2��g��=3CO2��g��+4H2O��l�� ��H =-2221.5 kJ��mol-1֪������C3H8��ȼ���� Ϊ2221.5 kJ��mol-1
Ϊ2221.5 kJ��mol-1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com