
【题目】氟离子电池是新型电池中的一匹黑马,其理论比能量高于锂电池。一种氟离子电池的工作原理如图所示。下列说法正确的是
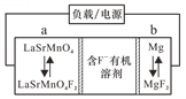
A.放电时,b是电源的正极
B.放电时,a极的电极反应为:LaSrMnO4F2+2e-=LaSrMnO4+2F-
C.充电时,电极a接外电源的负极
D.可将含F-的有机溶液换成水溶液以增强导电性
【答案】B
【解析】
由于Mg是活泼金属,Mg2+氧化性弱,所以该电池工作时Mg失去电子结合F-生成MgF2,即b电极为负极,电极反应式为:Mg+2F--2e-=MgF2,则a为正极,正极反应式为:LaSrMnO4F2+2e-=LaSrMnO4+2F-;充电时,电解池的阳极、阴极与原电池的正、负极对应,电极反应与原电池的电极反应反应物与生成物相反,据此解答。
A.由于Mg是活泼金属,Mg2+氧化性弱,所以原电池放电时,Mg失去电子,作负极,即b为负极,a为正极,A错误;
B.放电时,a为正极发生还原反应,电极反应为:LaSrMnO4F2+2e-=LaSrMnO4+2F-,B正确;
C.充电时电解池的阳极、阴极与原电池的正、负极对应,所以a极接外电源的正极,C错误;
D.因为Mg能与水反应,因此不能将有机溶液换成水溶液,D错误;
答案选B。


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】铜和镁的合金4.6 g完全溶于浓硝酸,若反应中硝酸被还原只产生4 480 mL NO2气体和336 mL的N2O4气体(气体的体积已折算到标准状况),在反应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质量为 ( )
A.9.02 gB.8.51 gC.8.26 gD.7.04 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】300 ℃时,将2 mol A和2 mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g) ![]() 2C(g)+2D(g)ΔH=Q,2 min末达到平衡,生成0.8 mol D。
2C(g)+2D(g)ΔH=Q,2 min末达到平衡,生成0.8 mol D。
(1)300 ℃时,该反应的平衡常数表达式为:K=______。已知K300 ℃<K350 ℃,则ΔH______0(填“>”或“<”)。
(2)若温度不变,缩小容器容积,则A的转化率________(填“增大”“减小”或“不变”),原因是_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤炭燃烧时产生大量SO2、NO对环境影响极大。
(1)使用清洁能源可有效减少SO2等的排放。煤的液化是现代能源工业中重点推广的能源综合利用方案,最常见的液化方法为用煤生产CH3OH。已知制备甲醇的有关化学反应及平衡常数如下:
i:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH1=-a kJ/mol
CH3OH(g)+H2O(g) ΔH1=-a kJ/mol
ii:CO2(g)+H2(g) ![]() CO(g)+H2O(g) ΔH2=+b kJ/mol
CO(g)+H2O(g) ΔH2=+b kJ/mol
iii:CO(g)+2H2(g) ![]() CH3OH(g) ΔH3
CH3OH(g) ΔH3
ΔH3=________。
(2)在密闭容器中进行反应i,改变温度时,该反应中的所有物质都为气态,起始温度、体积相同(T1 ℃、2 L密闭容器)。反应过程中部分数据见下表:
反应时间 | CO2/mol | H2/mol | CH3OH/mol | H2O/mol | |
反应Ⅰ恒 温恒容 | 0 min | 2 | 6 | 0 | 0 |
10 min | 4.5 | ||||
20 min | 1 | ||||
30 min | 1 | ||||
反应Ⅱ绝 热恒容 | 0 min | 0 | 0 | 2 | 2 |
①达到平衡后,反应Ⅰ、Ⅱ对比:平衡常数K(Ⅰ)________K(Ⅱ)(填“>”“<”或“=”下同);平衡时CO2的浓度c(Ⅰ)________c(Ⅱ)。
②对反应Ⅰ,在其他条件不变下,若30 min时只改变温度为T2 ℃,再次平衡时H2的物质的量为2.5 mol,则T1________T2(填“>”“<”或“=”)。
③若30 min时只向容器中再充入1 mol H2(g)和1 mol H2O(g),则平衡________移动(填“正向”“逆向”或“不”)。
(3)研究人员发现,将煤炭在O2/CO2的气氛下燃烧,能够降低燃煤时NO的排放,主要反应为:2NO(g)+2CO(g)=N2(g)+2CO2(g)。在一定温度下,于2 L的恒容密闭容器中充入0.1 mol NO和0.3 mol CO发生该反应,如图为容器内的压强(p)与起始压强(p0)的比值(p/p0)随时间的变化曲线。
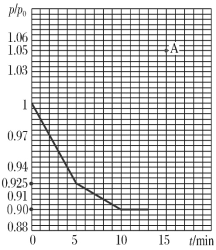
①0~5 min内,该反应的平均反应速率v(NO)=________;平衡时N2的产率为________。
②若13 min时,向该容器中再充入0.06 mol CO2,15 min时再次达到平衡,此时容器内![]() /
/![]() 的比值应在图中A点的________(填“上方”或“下方”)。
的比值应在图中A点的________(填“上方”或“下方”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用下图所示装置进行液体石蜡分解及其产物性质实验。下列操作或叙述错误的是
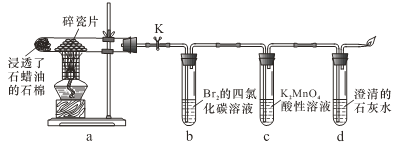
A.装置b、c中发生反应的基本类型不同
B.实验中可能看不到b、c中溶液明显褪色
C.d中溶液变浑浊证明石蜡分解产生了CO2
D.停止加热后立即关闭K可以防止液体倒吸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LED产品具有耗电量低、寿命长的特点。下图是氢氧燃料电池驱动LED屏发光的装置,下列有关叙述错误的是( )
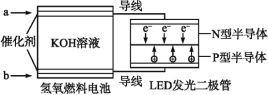
A.a处通入的气体是氢气,电极反应式为H2+2OH-2e=2H2O
B.装置中电子的流向为a极→N型半导体→P型半导体→b极
C.装置中的能量转化至少涉及三种形式的能量
D.图中![]() 表示来自氢氧燃料电池中的K+的移动方向
表示来自氢氧燃料电池中的K+的移动方向
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】贝壳、珍珠、方解石等主要成分均含有CaCO3,回答下列问题:
(1)利用焰色反应的原理既可制作五彩缤纷的节日烟花,亦可定性鉴别某些金属盐。灼烧碳酸钙时的焰色为_______(填标号)。
A 黄色 B 红色 C 紫色 D 绿色
(2)CaCO3中三种元素第一电离能由小到大的顺序是__________。CaCO3中的化学键除了σ键外,还存在_________________。
(3)关于CO2和CO32-的下列说法正确的是__________。
a 两种微粒价层电子对数相同 b 两种微粒的中心原子均无孤电子对
c 键角:CO2>CO32- d 两种微粒的中心原子杂化方式相同
(4)难溶碳酸盐易分解,CaCO3、BaCO3热分解温度更高的是_____,原因是______。
(5)方解石的菱面体结构如图1,沿三次轴的俯视图为正六边形。方解石的六方晶胞结构如图2,晶胞底面为平行四边形,其较小夹角为60°,边长为anm,晶胞高为c nm。
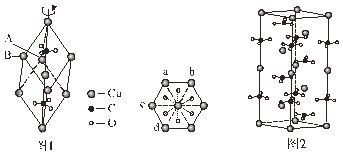
A点在俯视图中为a,则B点在俯视图中的位置为_________(填字母)。方解石的六方晶胞中,Ca2+和CO32-个数比为___________;若阿伏加德罗常数为NA,则该方解石的密度为________g/cm3(列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下有①6.72LCH4;②3.01x1023个HCl;③13.6gH2S;④0.2molNH3。下列对四种气体的关系从小到大表示不正确的是( )
A.体积:④<①<②<③
B.密度:①<④<③<②
C.质量:④<①<③<②
D.氢原子数:②<④<③<①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、某化学研究性学习小组为探究元素性质的变化规律,设计了如下实验:
(1)甲同学欲比较N、C、Si的非金属性强弱,设计了图1所示的实验装置,其设计的依据是 ;但该装置存在缺陷,请指出 。
(2)乙同学设计了如图2装置验证元素性质递变规律。A、B、C处分别是蘸有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润的红纸。乙同学可能观察到的现象
A. ;B. ;C. 。
从环保角度考虑,该装置有明显不足,请指出提出改进建议 。
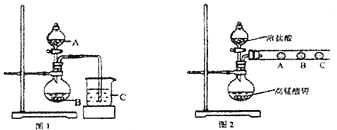
Ⅱ、另一化学研究性学习小组在实验室条件下用以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯,并对阳极泥和电解液中金属进行回收和含量测定。已知粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不反应)。
步骤一:电解精制:电解时,粗铜应与电源的 极相连。阴极上的电极反应式为 。
步骤二:电解完成后,该小组同学按以下流程对电解液进行处理:

(1)阳极泥的综合利用:稀硝酸处理阳极泥得到硝酸银稀溶液,请写出该步反应的离子方程式: 。
残渣含有极少量的黄金,如何回收金,他们查阅了有关资料,了解到了一些有关金的信息:
序号 | 反应 | 平衡常数 |
1 |
|
|
2 |
|
|
请根据以上信息简要解释溶解阳极泥不用王水的原因 。
(2)滤液含量的测定:以下是该小组探究滤液的一个实验流程。
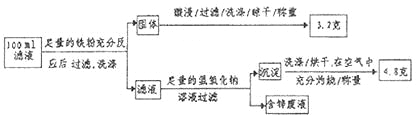
则![]() 滤液中
滤液中![]() 的浓度为
的浓度为 ![]() ,
,![]() 的浓度为
的浓度为 ![]() 。
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com