
| A. | 常温常压下,48gO3中所含的氧原子数为3NA | |
| B. | 1.8gNH4+中所含质子数为0.1NA | |
| C. | 标况下,11.2L氧气中所含原子数为0.5NA | |
| D. | 2.4g金属镁变成离子时得到的电子数为0.2NA |
分析 A.臭氧由氧原子构成,依据n=$\frac{m}{M}$计算解答;
B.质量转化为物质的量,结合一个铵根离子含有含有11个质子;
C.计算氧气的物质的量结合1个氧气分子含有2个氧原子解答;
D.质量转化为物质的量结合1个镁原子失去2个电子转化为镁离子.
解答 解:A.常温常压下,48gO3中所含的氧原子数为$\frac{48g}{16g/mol}$×3×NA=3NA,故A正确;
B.1.8gNH4+中所含质子数为$\frac{1.8g}{18g/mol}$×11×NA=0.11NA,故B错误;
C.标况下,11.2L氧气中所含原子数为$\frac{11.2L}{22.4L/mol}$×2×NA=NA,故C错误;
D.2.4g金属镁物质的量为0.1mol,变成离子时失去的电子数为0.2NA,故D错误;
故选:A.
点评 本题考查了阿伏伽德罗常数的分析判断,掌握物质的量与阿伏伽德罗常数、摩尔质量等之间的转化关系是解题关键,注意气体摩尔体积的适用对象和条件,注意金属单质在反应中失去电子生成阳离子,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 一定是碱溶液 | B. | 一定是酸溶液 | ||
| C. | 由水电离出的[OH-]=1×10-9mol•L-1 | D. | pH值可能为9也可能为5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含NA个N2和O2的混合气体中质子数不可能是15NA | |
| B. | 1 L 1 mol•L-1的CH3COONa溶液中CH3COOH和CH3COO-的总数为NA | |
| C. | 58g 分子式为C4H10的有机物中,所含有的甲基数一定为2NA | |
| D. | NA个CH4和NA个Cl2光照下充分反应,被取代的氢原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
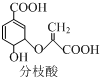 ,下列关于分枝酸的说法不正确的是( )
,下列关于分枝酸的说法不正确的是( )| A. | 分子中含有3种含氧官能团 | |
| B. | 1 mol分枝酸最多可与3mol NaOH发生中和反应 | |
| C. | 在一定条件下可与乙醇、乙酸反应,且反应类型相同 | |
| D. | 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,但褪色原理不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K2S溶液中:SO42-、K+、Cl-、Cu2+ | |
| B. | 无色溶液中:Fe2+、Na+、ClO-、Cl- | |
| C. | 室温下,$\frac{KW}{c({H}^{+})}$=0.1mol•L-1的溶液中:Na+、K+、SiO32-、NO3- | |
| D. | 滴入KSCN溶液显红色的溶液中:K+、Na+、SO42-、C6H5OH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
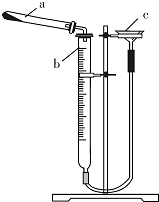 碱式碳酸铜是一种具有广泛用途的化工产品,主要用于固体荧光粉激活剂和铜盐的制造等.
碱式碳酸铜是一种具有广泛用途的化工产品,主要用于固体荧光粉激活剂和铜盐的制造等.| 实验序号 | 样品质量/g | CO2体积/mL(已折算成标准状况下) |
| 1 | 0.542 | 44.82 |
| 2 | 0.542 | 44.80 |
| 3 | 0.542 | 44.78 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ZnCl2是氧化产物,又是还原产物 | |
| B. | ZnI2是氧化产物,又是还原产物 | |
| C. | ICl跟H2O的反应,ICl是氧化剂,H2O是还原剂 | |
| D. | ICl跟H2O的反应,是自身氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在含有大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- | |
| B. | 25℃,在c(H+)=10-13mol/L的溶液中:NH4+、Al3+、SO42-、NO3- | |
| C. | 能使广泛pH试纸显蓝色的溶液中:Na+、K+、AlO2-、CO32- | |
| D. | 25℃,在pH=0的溶液中:K+、Fe2+、Cl-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com