
| A. | 4.32 g | B. | 4.68 g | C. | 5.36 g | D. | 6.38 g |
分析 硝酸被还原为NO气体且标准状况下体积为0.896L,即物质的量为0.04mol,根据氮元素的化合价变化计算转移电子物质的量,最后沉淀为Cu(OH)2、Mg(OH)2,金属提供的电子的物质的量等于氢氧根离子的物质的量,故最后沉淀质量等于金属的质量加氢氧根离子的质量.
解答 解:硝酸被还原为NO气体且标准状况下体积为0.896L,物质的量为:$\frac{0.896L}{22.4L/mol}$=0.04mol,所以转移的电子的物质的量为:0.04mol×(5-2)=0.12mol,
最后沉淀为Cu(OH)2、Mg(OH)2,金属提供的电子的物质的量等于氢氧根离子的物质的量,则沉淀中氢氧根离子的物质的量为0.12mol,
所以最后沉淀质量为:2.64g+0.12mol×17g/mol=4.68g.
故选B.
点评 本题考查混合物的计算,难度中等,明确反应发生的实质为解答关键,注意掌握守恒思想在化学计算中的应用,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 它们形成的简单离子若带有同种电荷,则电荷越多半径越大 | |
| B. | 它们之间既有可能形成离子化合物,又有可能形成共价化合物 | |
| C. | 它们形成的简单离子,阴离子半径必定大于阳离子半径 | |
| D. | 它们形成的简单离子,可能具有相同的电子层结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ①②③ | C. | ②③⑤ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4与Cl2的混合气体光照后颜色变浅 | |
| B. | 苯加入溴水中用力振荡,静止后水层变为无色 | |
| C. | C2H4通入酸性KMnO4溶液中,溶液紫色逐渐变浅 | |
| D. | C2H4通入Br2的CCl4溶液中,溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 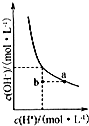 如图为在水溶液中H+和OH-的浓度变化曲线,恒温稀释可实现a→b的转化 | |
| B. |  如图为H2O2在有、无催化剂下的分解反应曲线b表示有催化剂时的反应 | |
| C. | 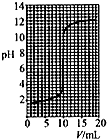 如图可表示用0.0110mol/L盐酸滴定0.0110mol/L氨水时的滴定曲线 | |
| D. | 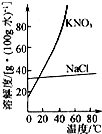 如图为NaCl中含有少量KNO3,可在较高温度下制得浓溶液再冷却结晶、过滤、干燥 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com