
| A. | 制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料 | |
| B. | 严禁在写作业时将铅笔放入口中啃咬,否则会引起铅中毒 | |
| C. | 工业冶炼铝时电解Al2O3并加入冰晶石(Na3AlF6),是为了降低Al2O3的熔融温度 | |
| D. | 洗衣粉中添加三聚磷酸钠,增强去污的效果 |
科目:高中化学 来源: 题型:选择题
| A. | 提高高锰酸钾的氧化能力,用浓盐酸酸化 | |
| B. | 抑制Fe2+ 的水解,用稀硝酸酸化 | |
| C. | 检验某卤代烃中是否含氯元素,先加HNO3酸化,再加AgNO3溶液检验. | |
| D. | 确认溶液中含有SO42- 时,先用过量盐酸酸化,再加BaCl2溶液检验. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对于反应Na2SO3+H2SO4═Na2SO4+SO2↑+H2O,增大体系的压强 | |
| B. | 对于N2(g)+3H2(g)?2NH3(g),容器体积固定不变时,充入Ar | |
| C. | 对于N2(g)+3H2(g)?2NH3(g),容器体积固定不变时,充入N2 | |
| D. | 对于N2(g)+3H2(g)?2NH3(g),容器气体压强不变时,充入Ar |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
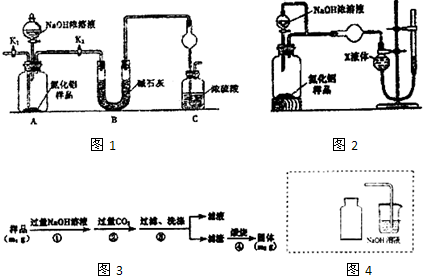

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合反应 | B. | 消去反应 | C. | 加成反应 | D. | 加聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com