
科目:高中化学 来源: 题型:
实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | NaOH溶液 | ||
1 | 20.2 | 20.3 | 23.7 |
2 | 20.3 | 20.5 | 23.8 |
3 | 21.5 | 21.6 | 24.9 |
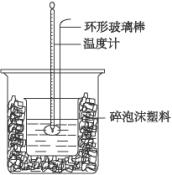
试回答下列问题:
(1)实验时用环形玻璃棒搅拌溶液的方法是_______________________,不能用铜丝搅拌棒代替环形玻璃棒的理由是_____________________________________________。
(2)经数据处理,t2-t1=3.4 ℃。则该实验测得的中和热ΔH=_________________〔盐酸和NaOH溶液的密度按1 g·Cm-3计算,反应后混合溶液的比热容C按4.18 J·(g·℃)-1计算〕。
(3)若将NaOH溶液改为相同中体积、相同浓度的氨水,测得中和热为ΔH1,则ΔH1与ΔH的关系为:ΔH1___ΔH(填“<”“>”或“=”=,理由是:__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验次数 | 起始温度t1/℃ | 止温度t2/℃ | |
盐酸 | NaOH溶液终 | ||
1 | 20.2 | 20.3 | 23.7 |
2 | 20.3 | 20.5 | 23.8 |
3 | 21.5 | 21.6 | 24.9 |
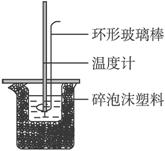
试完成下列问题:
(1)实验时用环形玻璃棒搅拌溶液的方法是________________________,不能用铜丝搅拌棒代替环形玻璃棒的理由是________________________________。
(2)经数据处理,t2-t1=3.4 ℃。则该实验测得的中和热ΔH=________________〔盐酸和NaOH溶液的密度按1 g·cm-3计算,反应后混合溶液的比热容(c按4.18 J·(g·℃)-1计算)〕。
(3)若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和热为ΔH1,则ΔH1与ΔH的关系为:ΔH1_____ΔH(填“<”“>”或“=”),理由是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | NaOH溶液 | ||
1 | 20.2 | 20.3 | 23.7 |
2 | 20.3 | 20.5 | 23.8 |
3 | 21.5 | 21.6 | 24.9 |
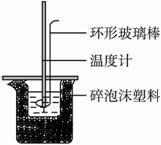
试回答下列问题:?
(1)实验时用环形玻璃棒搅拌溶液的方法是________________,不能用铜丝搅拌棒代替环形玻璃棒的理由是_________________________。
(2)经数据处理,t2-t1=3.4 ℃。则该实验测得的中和热ΔH=________________〔盐酸和NaOH溶液的密度按1 g·cm-3计算,反应后混合溶液的比热容(c按4.18 J·g-1·℃-1计算)〕。
(3)若将NaOH溶液改为相同中体积、相同浓度的氨水,测得中和热为ΔH1,则ΔH1与ΔH的关系为:ΔH1ΔH(填“<”“>”或“=”),理由是__________________________。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年云南省昆明市官渡区二中高二9月月考化学试卷(带解析) 题型:实验题
(共6分)实验室用50 mL 0.50 mol·L-1盐酸、50 mL 0.55 mol·L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到表中的数据: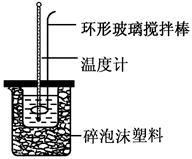
| 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | NaOH溶液 | ||
| 1 | 20.2 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com