
ŹÆ»ŅŹÆµÄ·Ö½ā·“Ó¦ĪŖ£ŗCaCO3(s)==CaO(s) +CO2(g)
Ęä”÷H£Ø298K£©==178.2kJ·mol—£±£¬”÷S£Ø298K£©== 169.6J·mol—1·K—1
169.6J·mol—1·K—1
ŹŌøł¾ŻŅŌÉĻŹż¾ŻÅŠ¶ĻøĆ·“Ó¦ŌŚ³£ĪĀĻĀŹĒ·ń×Ō·¢½ųŠŠ£æĘä·Ö½āĪĀ¶ČŹĒ¶ąÉŁ£æ
 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓŠNa2SO4ŗĶFe2(SO4)3µÄ»ģŗĻČÜŅŗ£¬ŅŃÖŖĘäÖŠFe3£«µÄĪļÖŹµÄĮæÅضČĪŖ0.4 mol/L£¬SO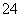 µÄĪļÖŹµÄĮæÅضČĪŖ0.7 mol/L£¬Ōņ“ĖČÜŅŗÖŠNa£«µÄĪļÖŹµÄĮæÅضČĪŖ (””””)
µÄĪļÖŹµÄĮæÅضČĪŖ0.7 mol/L£¬Ōņ“ĖČÜŅŗÖŠNa£«µÄĪļÖŹµÄĮæÅضČĪŖ (””””)
A£®0.1 mol/L B£®0.15 mol/L
C£®0.2 mol/L D£®0.25 mol/L
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻÖÓŠĻĀĮŠĪļÖŹ£ŗ¢ŁNa2CO3 ¢ŚĶ ¢ŪĀČ»ÆĒā ¢ÜCO2 ¢ŻNaHSO4 ¢ŽBa(OH)2 ¢ßĒāŃõ»ÆĢś½ŗĢå ¢ą°±Ė® ¢įĻ”ĻõĖį ¢āKI
 £Ø1£©°“ĪļÖŹµÄ·ÖĄą·½·ØĢīŠ“±ķøńµÄæհד¦(ĢīĪļÖŹ±ąŗÅ)
£Ø1£©°“ĪļÖŹµÄ·ÖĄą·½·ØĢīŠ“±ķøńµÄæհד¦(ĢīĪļÖŹ±ąŗÅ)
| ·ÖĄą±ź×¼ | µē½āÖŹ | ŃĪ | ·Ēµē½āÖŹ | »ģŗĻĪļ |
| ŹōÓŚøĆĄą µÄĪļÖŹ |
£Ø2£©ÉĻŹöijĮ½ÖÖĪļÖŹŌŚČÜŅŗÖŠæÉ·¢ÉśĄė×Ó·“Ó¦£ŗH£«£«OH£= H2O£¬Š“³öĘäÖŠŅ»øöøĆĄė×Ó·“Ó¦¶ŌÓ¦µÄ»Æѧ·½³ĢŹ½ ”£
£Ø3£©ĪļÖŹ¢āµÄĻ”ČÜŅŗŌŚæÕĘųÖŠ±»Ńõ»Æ£¬¼ÓČėµķ·ŪČÜŅŗĻŌĄ¶É«£¬Ōņ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ

 £¬
£¬
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ņ»¶ØĪĀ¶ČĻĀŌŚŅ»ČŻ»ż²»±äµÄĆܱÕČŻĘ÷ÖŠ·¢ÉśæÉÄę·“Ó¦2X(g)  Y(g)£«Z(s)£¬ŅŌĻĀ²»ÄÜĖµĆ÷øĆ·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄŹĒ (””””)
Y(g)£«Z(s)£¬ŅŌĻĀ²»ÄÜĖµĆ÷øĆ·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄŹĒ (””””)
A£®»ģŗĻĘųĢåµÄĆÜ¶Č²»ŌŁ±ä»Æ
B£®·“ӦȯĘ÷ÖŠYµÄÖŹĮæ·ÖŹż²»±ä
C£®XµÄ·Ö½āĖŁĀŹÓėYµÄĻūŗÄĖŁĀŹĻąµČ
D£®µ„Ī»Ź±¼äÄŚÉś³É1 mol YµÄĶ¬Ź±Éś³É2 mol X
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚŅ»¶ØĪĀ¶ČĻĀæÉÄę·“Ó¦N2+3H2 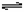 2NH3ŅŃ“ļµ½Ę½ŗā£¬
2NH3ŅŃ“ļµ½Ę½ŗā£¬
ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄ £Ø £©
¢Ł 1øöN”ŌN¼ü¶ĻĮѵÄĶ¬Ź±£¬ÓŠ3øöH—H¼üŠĪ³É ¢Ś ·“Ó¦»ģŗĻĪļÖŠø÷×é·ÖµÄĢå»ż·ÖŹż±£³Ö²»±ä
¢Ū ŗćĪĀŗćČŻŹ±£¬ČŻĘ÷ÄŚµÄŃ¹Ēæ²»ŌŁøÄ±ä ¢Ü 1øöN”ŌN¼ü¶ĻĮѵÄĶ¬Ź±£¬ÓŠ3øöN—H ¼üŠĪ³É
¢Ż NH3Éś³ÉµÄĖŁĀŹÓėNH3·Ö½āµÄĖŁĀŹĻąµČ ¢Ž µ„Ī»Ź±¼äÉś³Én molN2£¬Ķ¬Ź±Éś³É2n molNH3
¢ß ĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ²»ŌŁøÄ±ä ¢ą N2 H2 NH3µÄ·Ö×ÓŹżŅ»¶ØĪŖ1”Ć3”Ć2
¢į ŗćĪĀŗćČŻŹ±£¬ĘųĢåµÄ×ÜĪļÖŹµÄĮæ²»ŌŁøÄ±ä ¢ā ŗćĪĀŗćŃ¹Ź±£¬ČŻĘ÷ÄŚµÄĆÜ¶Č²»ŌŁøıä
A£®¢Ł¢Ś¢Ū¢Ü¢Ż¢Ž¢ß¢į B£®¢Ł¢Ś¢Ū¢Ż¢Ž¢ā C£® ¢Ū¢Ü¢Ż¢Ž¢ß ¢ą D£®¢Ł¢Ś¢Ū¢Ż¢Ž¢ß¢į¢ā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
øßĪĀĻĀ£¬Ä³·“Ó¦“ļĘ½ŗā£¬Ę½ŗā³£Źż
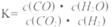
 ŗćČŻŹ±£¬ĪĀ¶ČÉżøߣ¬H2ÅØ¶Č¼õŠ””£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
ŗćČŻŹ±£¬ĪĀ¶ČÉżøߣ¬H2ÅØ¶Č¼õŠ””£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®øĆ·“Ó¦µÄģŹ±äĪŖÕżÖµ
B£®ŗćĪĀŗćČŻĻĀ£¬Ōö“óŃ¹Ē棬H2ÅضČŅ»¶Ø¼õŠ”
C£®ÉżøßĪĀ¶Č£¬Äę·“Ó¦ĖŁĀŹ¼õŠ”
 D£®øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖCO+ H2O CO2+H2
D£®øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖCO+ H2O CO2+H2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
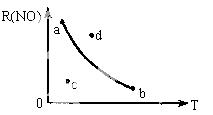
ČēĶ¼£¬Ģõ¼žŅ»¶ØŹ±£¬·“Ó¦2NO(g)+O2(g)  2NO2(g)+Q£ØÕż·“Ó¦ĪŖ·ÅČČ£©ÖŠNOµÄRmaxÓėT±ä»Æ¹ŲĻµĒśĻßĶ¼£¬Ķ¼ÖŠÓŠa”¢b”¢c”¢d4øöµć£¬ĘäÖŠ±ķŹ¾Ī““ļµ½Ę½ŗāדĢ¬£¬ĒŅ¦ĶÕż<¦ĶÄęµÄµćŹĒ£Ø £©
2NO2(g)+Q£ØÕż·“Ó¦ĪŖ·ÅČČ£©ÖŠNOµÄRmaxÓėT±ä»Æ¹ŲĻµĒśĻßĶ¼£¬Ķ¼ÖŠÓŠa”¢b”¢c”¢d4øöµć£¬ĘäÖŠ±ķŹ¾Ī““ļµ½Ę½ŗāדĢ¬£¬ĒŅ¦ĶÕż<¦ĶÄęµÄµćŹĒ£Ø £©
A£®a B£®b C£®c D£®d
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĪļÖŹÖŠ“ęŌŚĖ³·“Ņģ¹¹ĢåµÄŹĒ
A£®2£ĀȱūĻ© ”””” B£®±ūĻ© ”””” C£®2£¶”Ļ© ”” D£®1£¶”Ļ©
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com