
【题目】将足量的甲和乙组成的混合气体通入丙溶液,一定能产生沉淀的是
甲 | 乙 | 丙 | |
A. | NO2 | SO2 | BaCl2 |
B. | HC1 | CO2 | 石灰水 |
C. | CO2 | SO2 | 石灰水 |
D. | CO2 | NH3 | CaCl2 |
A. A B. B C. C D. D
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案科目:高中化学 来源: 题型:
【题目】取一定质量含Cu、Cu2O、CuO的固体混合物,将其分成两等份并进行下列转化, 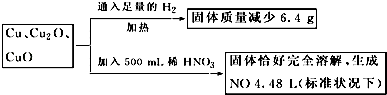
则转化过程中所加稀HNO3的物质的量浓度为( )
A.4.4 molL﹣1
B.3.6 molL﹣1
C.4.0 molL﹣1
D.3.2 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在容积为0.1L的密闭容器中,通入0.4molN2和1.2molH2,进行反应,2s后达到平衡,此时容器内的压强为起始时的3/4,试回答:
(1)能判断该反应达到平衡状态的依据是___________
A.断开3molH—H键的同时断开2molN—H键 B.c(N2) : c(H2): c(NH3) =1:3:2
C.混合气体的平均相对分子质量不变 D.容器内密度不变
(2)N2的转化率α1%=_________,若相同条件下,此反应在容积可变的容器中进行,保持压强不变,达到平衡,则N2的转化率α2%________α1%(填“>”、“<”或“=”)
(3)该温度下,反应的化学平衡常数K=__________,若此时再加入0.6molN2和0.4mol NH3,则平衡_______________(填“向左移动”、“向右移动”或“不移动”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列化学反应中,即有离子键、极性键、非极性键断裂,又有离子键、极性键、非极性键形成的是
A. 2Na2O2 +2H2O= 4NaOH +O2↑ B. SO2+2H2S=3S+2H2O
C. Mg3N2+6H2O=3Mg (OH) 2↓+2NH3↑ D. C+O2= CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A,B,C,D,E五种元素,其中A,B,C属于同一周期,A原子最外层p能级的电子数等于次外层的电子总数;B原子最外层中有两个不成对的电子;D,E原子核内各自的质子数与中子数相等;B元素可分别与A,C,D,E生成RB2型化合物,并知在DB2和EB2中,D与B的质量比为7:8;E与B的质量比为1:1.试回答:
(1)写出D原子的电子排布式 .
(2)用电子式表示AE2的形成过程 .
(3)B,C两元素的第一电离能大小关系为>(填元素符号),原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲~辛等元素在周期表中的相对位置如图.甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( ) 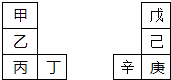
A.金属性:甲>乙>丁
B.原子半径:辛>己>戊
C.丙与庚的原子核外电子数相差13
D.乙的单质在空气中燃烧生成只含离子键的化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com