
海藻中含有丰富的碘元素 (以I-形式存在)。实验室中提取碘的流程如下:
 |
(1) 实验操作③的名称是__________,所用主要仪器名称为__________。
(2) 提取碘的过程中,可供选择的有机试剂是__________(填序号)。
A、酒精(沸点78 ℃) B、四氯化碳(沸点77 ℃)
C、甘油(沸点290 ℃) D、苯(沸点80 ℃)
(3)在操作②中,溶液中生成少量ICl,为消除此杂质,使碘全部游离出来,应加入适量(填序号)__________溶液,反应的离子方程式为______________________。
A、KIO3 B、HClO C、KI D、Br2
(4)为使从含碘有机溶液中提取碘并回收溶剂顺利进行,采用水浴加热蒸馏(如图所示)。 请指出图中实验装置中错误之处(有几处填几处,下列空白可不填满,也可补充)。
 |
①____________________________, ②____________________________,③____________________________, ④____________________________。
(5)实验中使用水浴的原因是 ,最后晶体碘聚集在
__________(填仪器名称)中。
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:
短周期元素W、X、Y、Z的原子序数依次增大,其简单离子都能破坏水的电离平衡的是( )
A.W2- X+ B.X+ Y3+
C.Y3+ Z2- D.X+ Z2-
| R | |||
| T | Q | W |
查看答案和解析>>
科目:高中化学 来源: 题型:
亮菌甲素为利胆解痉药适用于急性胆囊炎治疗等,其结构简式如右图所示
 下列有关叙述正确的是
下列有关叙述正确的是
A.亮菌甲素分子式为C12H11O5
B.亮菌甲素能与三氯化铁溶液发生显色反应,1mol最多能与5molH2发生加成反应
C.1mol亮菌甲素在一定条件下与NaOH溶液完全反应最多能消耗2mol NaOH
D.每个亮菌甲素分子在一定条件下与足量H2反应后的产物有3个手性碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
1~20号元素(稀有气体元素除外)中:
(1)原子半径最小的 ,是原子半径最大的是 。
(2)与水反应最剧烈的金属单质是 ,非金属单质是 。
(3)既能与酸反应,又能与碱反应的金属单质是 。
(4)硬度最大的单质是 。
(5)气态氢化物的水溶液酸性最强的是 。
(6)最高价氧化物对应的水化物碱性最强的是 。(以上填元素符号)
(7)铅是碳的同族元素,比碳多4个电子层,铅在周期表的位置为 周期、第 族。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于仪器使用的说法正确的是( )
A.滴定管装滴定液时应先用滴定液润洗
B.锥形瓶用作反应容器时一定不能加热
C.蒸馏时温度计水银球可以高于蒸馏瓶支管口
D.振荡分液漏斗时应关闭其玻璃塞和活塞
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上常利用含硫废水生产Na2S2O3·5H2O,实验室可用如下装置(略去部分夹持仪器)模拟生产过程。
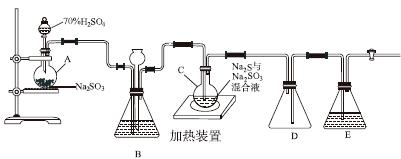
烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)===Na2SO3(aq)+H2S(aq) (Ⅰ)
2H2S(aq)+SO2(g)===3S(s)+2H2O(l) (Ⅱ)
S(s)+Na2SO3(aq) Na2S2O3(aq) (Ⅲ)
Na2S2O3(aq) (Ⅲ)
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若________________,则整个装置气密性良好。装置D的作用是__________。装置E中为________溶液。
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为________。
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择________。
a.蒸馏水 b.饱和Na2SO3溶液
c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
实验中,为使SO2缓慢进入烧瓶C,采用的操作是__________________________。已知反应(Ⅲ)相对较慢,则烧瓶C中反应达到终点的现象是__________________。反应后期可用酒精灯适当加热烧瓶A,实验室用酒精灯加热时必须使用石棉网的仪器还有________。
a.烧杯 b.蒸发皿
c.试管 d.锥形瓶
(4)反应终止后,烧瓶C中的溶液经蒸发浓缩、冷却结晶即可析出Na2S2O3·5H2O,其中可能含有Na2SO3、Na2SO4等杂质。利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作、现象和结论:________________________________________。
已知Na2S2O3·5H2O遇酸易分解:S2O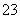 +2H+===S↓+SO2↑+H2O
+2H+===S↓+SO2↑+H2O
供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验能达到目的的是( )
A.只滴加氨水鉴别NaCl、AlCl3、MgCl2、Na2SO4四种溶液
B.将NH4Cl溶液蒸干制备NH4Cl固体
C.用萃取分液的方法除去酒精中的水
D.用可见光束照射以区别溶液和胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数,下列叙述中正确的是 ( )
A.标准状况下,2.24 L苯中约含有个NA碳原子
B.标准状况下,22.4 L H2中含中子数为2NA
C.1 L 1 mol/L醋酸溶液中离子总数为2NA
D.1 mol Mg与足量O2或N2反应生成MgO或Mg3N2均失去2NA个电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com