
【题目】溶液X中含有下表离子中的某5种,且其浓度均为0.1 mol·L1(不考虑水的电离与离子水解)。向X溶液中加入足量稀盐酸,有无色气体生成,经分析,反应前后阴离子种类没有变化。下列叙述不正确的是( )
阳离子 | 阴离子 |
Na+、Fe3+、Fe2+、Mg2+ | NO3-、HCO3-、CO32-、SO42-、Cl- |
A.X溶液中一定含Fe3+、Fe2+
B.X溶液中不可能含有HCO3-或CO32-
C.生成无色气体的离子方程式为:3Fe2+ +NO3-+4H+===3Fe3++NO ↑ +2H2O
D.根据电荷守恒,原溶液中一定含Mg2+
【答案】A
【解析】
各种离子的物质的量浓度均为0.1mol/L,向溶液X中加入足量的盐酸,有气体生成,且阴离子种类不变,若是![]() 或
或![]() ,则阴离子种类会改变,所以溶液不可能有
,则阴离子种类会改变,所以溶液不可能有![]() 、
、![]() ;根据表中的离子,可以推知是
;根据表中的离子,可以推知是![]() 、
、![]() 在酸性环境下生成一氧化氮,加入盐酸,溶液中阴离子种类不变,所以原来溶液中含有
在酸性环境下生成一氧化氮,加入盐酸,溶液中阴离子种类不变,所以原来溶液中含有![]() ,若只含有
,若只含有![]() 和
和![]() ,二者的浓度为0.1mol/L,根据电荷守恒是不可能的,所以还含有阴离子
,二者的浓度为0.1mol/L,根据电荷守恒是不可能的,所以还含有阴离子![]() ,由于总共含有5种离子,再根据电荷守恒可知还含有一种带有两个正电荷的
,由于总共含有5种离子,再根据电荷守恒可知还含有一种带有两个正电荷的![]() ,所以原溶液中含有的五种离子为:
,所以原溶液中含有的五种离子为:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,以此解答该题。
,以此解答该题。
A.溶液中一定有![]() ,根据电荷守恒,无
,根据电荷守恒,无![]() ,故A错误;
,故A错误;
B.有气体生成,且阴离子种类不变,若是![]() 或
或![]() ,则阴离子种类会改变,所以溶液不可能有
,则阴离子种类会改变,所以溶液不可能有![]() 、
、![]() ,故B正确;
,故B正确;
C.在酸性条件下,![]() 、
、![]() 发生氧化还原反应:3Fe2+ +NO3-+4H+===3Fe3++NO ↑ +2H2O,故C正确;
发生氧化还原反应:3Fe2+ +NO3-+4H+===3Fe3++NO ↑ +2H2O,故C正确;
D.根据电荷守恒定律,阴离子![]() ,已确定的阳离子有
,已确定的阳离子有![]() ,还含有一种带有两个正电荷的
,还含有一种带有两个正电荷的![]() ,故D正确;
,故D正确;
答案选A。


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
【题目】在一定温度下,某容积不变的密闭容器中,建立下列化学平衡:C(s)+H2O(g)![]() CO(g)+H2(g)。下列叙述中不能说明上述可逆反应已达到化学平衡状态的是( )
CO(g)+H2(g)。下列叙述中不能说明上述可逆反应已达到化学平衡状态的是( )
A. 体系的压强不再发生变化
B. v正(CO)=v逆(H2O)
C. 生成n mol CO的同时生成n mol H2
D. 1molH—H键断裂的同时断裂2molH—O键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上把Cl2通入冷NaOH溶液中制得漂白液(有效成分为NaClO)。某化学小组在一定温度下将氯气缓缓通入NaOH溶液中,模拟实验得到ClO-、ClO3-等离子的物质的量n(mol)与反应时间t(min)的关系曲线。下列说法错误的是
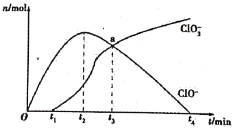
A.参加反应所需NaOH与氯气的物质的量之比一定为2:1
B.a点时溶液中n(NaCl):n(NaClO3):n(NaClO)=6:1:1
C.t2~t4,ClO-离子的物质的量下降的原因可能是3ClO-=2Cl-+ClO3-
D.使用漂白液时,为了增强漂白效果,可以向漂白液中通入二氧化硫
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。
实验一:他们利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来研究影响反应速率的因素。
甲同学研究的实验报告如下表:
实 验 步 骤 | 现 象 | 结 论 |
①分别取等体积的2 mol/L硫酸于试管中; | 反应快慢: | 反应物的性质越活泼, |
(1)该同学的实验目的是_________________________________________;
要得出正确的实验结论,还需控制的实验条件是_____________。
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用下图装置进行定量实验。完成该实验应选用的实验药品可以是(从题中所给药品中挑选)_________________________________________________________;
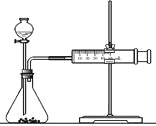
实验二:
已知: 2KMnO4+5H2C2O4+3H2SO4= K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
(1)针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是_______________的影响。
(2)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是__________________。
A.硫酸钾 B.硫酸锰 C.氯化锰 D.水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼镁泥是一种工业废料,主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O的流程如下:
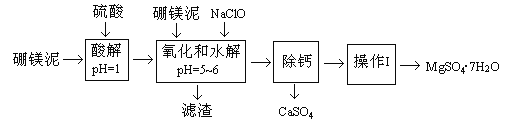
根据题意回答下列问题:
(1)实验中需用1mol/L的硫酸80mL,若用98%的浓硫酸来配制,除量筒、玻璃棒外,还需要的玻璃仪器有_________。
(2)滤渣的主要成份除含有Fe(OH)3、Al(OH)3、MnO2外,还有_________。
(3)加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式_________。在调节pH=5-6之前,还有一种离子也会被NaClO氧化,该反应的离子方程式为________________。
(4)如何检验滤液中Fe3+是否被除尽,简述检验方法_________。
(5)已知MgSO4、CaSO4的溶解度如下表:
温度(℃) | 40 | 50 | 60 | 70 |
MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明操作步骤_________、_________。
(6)如果提供的硼镁泥共100 g,得到的MgSO4·7H2O 196.8 g,则MgSO4·7H2O的产率为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由氯苯制取1,2,3,4一四氯己烷,步骤如下

(1)填写每步所属的反应类型(a.取代反应b.加成反应 c.消去反应,只需填写字母):①_________、②____________、③___________、④________、⑤__________
(2)反应②所需要的试剂和条件是_________________________;
(3)反应④⑤的化学方程式是④______________⑤________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 滴入酚酞显红色的溶液:Na+、NH4+、NO3-、Cl-
B. 0.1mol·L-1Fe(NO3)2溶液:H+、Al3+、SO42-、Cl-
C. 0.1mol·L-1氨水溶液:K+、Na+、NO3-、A1O2-
D. c(H+)/c(OH-)=1012mol·L-1的溶液:Ca2+、NH4+、Cl-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】活性炭吸附法是工业提碘的主要方法之一,其流程如图:
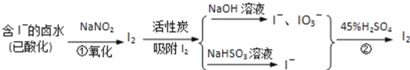
完成下列填空:
(1)酸性条件下,NaNO2溶液只能将I﹣氧化为I2,同时生成NO.写出反应①的离子方程式______.
(2)氯气、浓硝酸、酸性高锰酸钾等都是常用的强氧化剂,但工业上氧化卤水中的I﹣选择了价格并不便宜的亚硝酸钠,可能的原因是______.
(3)反应②发生时,溶液底部有紫黑色固体生成,有时溶液上方产生紫色气体,产生这种现象的原因是______.
(4)流程中,碘元素经过了I﹣→I2→I﹣、IO3﹣→I2的变化过程,这样反复操作的目的是______.
(5)流程中所用的NaHSO3溶液显弱酸性,源于NaHSO3存在以下两种程度不同的平衡体系:
①水解______和电离______(用离子方程式表示)
②如向0.1mol/L的NaHSO3溶液中分别加入以下物质,回答问题:
加入少量Ba(OH)2固体,水解平衡向______移动;加入少量NaClO固体,溶液的pH______(选填:增大、减小、不变).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种重要的化工原料,又是一种可再生能源,具有开发和应用的广阔前景。
(1)在一容积为2L的密闭容器内,充入0.2molCO与0.4molH2发生反应,CO(g)+2H2(g)![]() CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。
CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。

①A、B两点对应的压强大小关系是PA___PB(填“>、<、=”)。
②A、B、C三点的平衡常数KA,KB,KC的大小关系是___。
③下列叙述能说明上述反应能达到化学平衡状态的是___(填代号)。
a.H2的消耗速率是CH3OH生成速率的2倍 b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变 d.CO和CH3OH的物质的量之和保持不变
(2)在P1压强、T1℃时,该反应的平衡常数K=___。
(3)T1℃、1L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下,CO:0.1mol、H2:0.2mol、CH3OH:0.2mol,此时v(正)___v(逆)(填“>、<或=”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com