
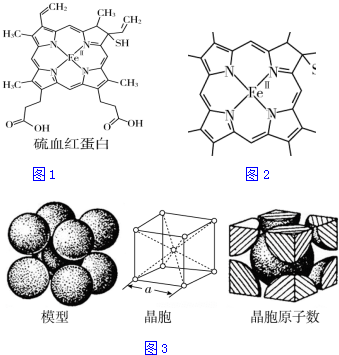
分析 (1)同一周期,自左而右电负性增大,同一主族,自上而下电负性减小;同主族,自上而下,元素的第一电离能减小,同一周期,自左而右元素的第一电离能增大,注意同一周期的第ⅡA元素的第一电离能大于第ⅢA族的,第ⅤA族的大于第ⅥA族的;
(2)具有相同原子数和最外层电子数的分子或离子叫等电子体,等电子体的结构和性质相似;分子间可以形成氢键使物质的粘度增大;
(3)根据C原子形成的σ键数目判断杂化类型;N原子最外层有5个电子,只需要形成3条键即可达到稳定结构,但是图中形成双键的N原子形成了四条键,显然有一条为配位键;(4)体心立方结构的配位数为8;利用均摊法计算晶胞的结构.
解答 解:(1)硫血红蛋白中所含非金属元素有:C、H、N、O、S,同周期元素从左到右元素的电负性逐渐增大,则有电负性C<N<O,H的电负性最小,所以电负性最大的是O;第一电离能最大的元素的原子是N;
故答案为:O;N;
(2)氧、硫属于同主族,CS2和CO2是等电子体,CO2具有直线型结构的分子,正、负电荷中心重合,是为非极性分子,等电子体的结构相似,CS2是非极性分子;硫酸分子中含有羟基,形成氢键,浓硫酸粘度较大的原因是分子间可以形成氢键;
故答案为:非极性;硫酸分子间可以形成氢键;
(3)甲基中C原子形成4个σ键,采取sp3杂化,形成双键的C原子形成3个σ键,采取sp2杂化;
N原子最外层有5个电子,只需要形成3条键即可达到稳定结构,但是图中形成双键的N原子形成了四条键,显然有一条为配位键,用“→”标出N和Fe2+形成的配位键为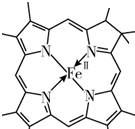 ;
;
故答案为:sp2、sp3; ;
;
(4)铁的金属密堆积方式为体心立方结构,晶胞中铁原子的配位数为8;体心立方中含有1+8×$\frac{1}{8}$=2个铁原子,晶胞中铁原子的体积为:2×$\frac{4}{3}$×π×r3,体心立方中,体对角线上为三个铁原子相切,则体对角线为4r,晶胞边长为:$\frac{4r}{\sqrt{3}}$,晶胞体积为:($\frac{4r}{\sqrt{3}}$)3,空间利用率为:$\frac{2×\frac{4}{3}×π×{r}^{3}}{(\frac{4r}{\sqrt{3}})^{3}}$=$\frac{\sqrt{3}π}{8}$,
故答案为:8;$\frac{\sqrt{3}π}{8}$.
点评 本题考查物质结构与性质,涉及元素性质递变规律、等电子原理应用、分子性质、配位键、晶胞计算等,(4)中计算为易错点、难点,需要学生具备一定的数学计算能力,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na、Mg、Al元素最高化合价依次升高 | |
| B. | P、Cl最高价氧化物对应的水化物酸性增强 | |
| C. | N、O、F元素非金属性依次减弱 | |
| D. | Li、Na、K原子的电子层数依次增多 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
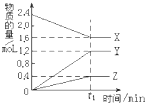 I.某温度下,在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图.反应在t1min时到达平衡,依图所示:
I.某温度下,在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图.反应在t1min时到达平衡,依图所示: 3Y+Z.
3Y+Z.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 某校课外实验小组同学设计如图装置进行实验.(夹持装置已略去).
某校课外实验小组同学设计如图装置进行实验.(夹持装置已略去).| 饱和醇的质量 | 金属钠的质量 | 量气管第一次读数 | 量气管第二次读数 | |
| ① | 0.62g | 5.0g(足量) | 40mL | 264mL |
| ② | 0.31g | 2.5g(足量) | 40mL | 152mL |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 维生素A的分子式为C20H32O | |
| B. | 维生素A可被催化氧化为醛 | |
| C. | 维生素A是一种易溶于水的醇 | |
| D. | 1mol维生素A在催化剂作用下最多可与7mol H2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜基态原子核外电子排布式为1s22s22p63s23p64s13d10 | |
| B. | 在d轨道中电子排布成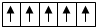 而不是 而不是 ,其最直接的根据是泡利原理 ,其最直接的根据是泡利原理 | |
| C. | 下列轨道的能量是按由高到低排列的E5s>E4s>E3d>E2p>E1s | |
| D. | 焰色反应、激光、霓虹灯光等与原子核外电子发生跃迁释放能量有关 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com