
����Ŀ���㶹�ؼ�����������ҽҩ��ũҩ��Ⱦ�Ƶ������й㷺��;��ij�㶹�����������п������������Ķ�����������ԣ���ϳ�·����ͼ��ʾ��
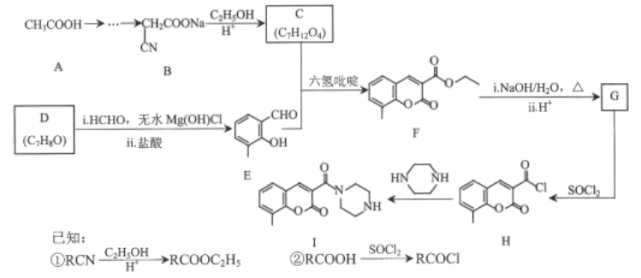 �ش��������⣺
�ش��������⣺
��1��D��������______��F�еĺ��������ŵ�������______��
��2��H��I�ķ�Ӧ����Ϊ______��
��3��C���Ӿ��жԳƽṹ���û�����Ľṹ��ʽΪ______��
��4��F��G��i�Ļ�ѧ����ʽΪ______��
��5��E��ͬ���칹���У�����������������______�֣�
�ٺ��б���
���ܷ���ˮ�ⷴӦ
���к˴Ź���������4����ҷ����֮��Ϊ3��2��2��1�Ľṹ��ʽΪ______��д��һ�ּ��ɣ���
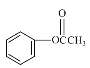
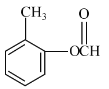
��6����������·�ߣ�����Ա��ӡ��Ҵ��������ᡢ��ȩΪԭ���Ʊ�![]() �ĺϳ�·��______���������Լ���ѡ����
�ĺϳ�·��______���������Լ���ѡ����
���𰸡��ڼױ��ӻ�2�������� ���� ȡ����Ӧ C2H5COCCH2COOC2H5 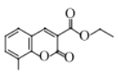 ��NaOH
��NaOH ![]()
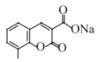 ��CH3CH2OH 6
��CH3CH2OH 6 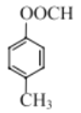 ��
�� ��
��
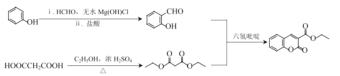
��������
(1)����D��E�Ľṹ��ʽ�Ա��Լ�D�ķ���ʽ��D�Ľṹ��ʽΪ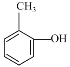 ���ó�D�����ƣ�����F�Ľṹ��ʽ���Ƴ����������ţ�
���ó�D�����ƣ�����F�Ľṹ��ʽ���Ƴ����������ţ�
(2)�Ա�H��I�Ľṹ��ʽ���ó���Ӧ���ͣ�
(3)������Ϣ�٣���C���Ӿ��жԳƽṹ���Ƴ�C�Ľṹ��ʽ��
(4)F�к����������ڼ���Һ�з���ˮ�⣻
(5)����E�Ľṹ����ˮ�⣬˵������������Ȼ����з�����
(1) ����D��E�Ľṹ��ʽ�Ա��Լ�D�ķ���ʽ��D�Ľṹ��ʽΪ ��D������Ϊ�ڼױ��ӻ�2�������ӣ�����F�Ľṹ��ʽ��F�к�����������������
��D������Ϊ�ڼױ��ӻ�2�������ӣ�����F�Ľṹ��ʽ��F�к�����������������
(2)�ԱȽṹ��ʽ��H�еġ�C��Cl�����������ѣ���һ��Ӧ����һ����N��H�����ѣ�����������Cl��H��ϳ�HCl�������ϳ�I���÷�Ӧ����Ϊȡ����Ӧ��
(3)������Ϣ�٣���CΪ�Գƽṹ���Ƴ�C�Ľṹ��ʽΪC2H5COCCH2COOC2H5��
(4)������Ϣ�ڣ��ó�G��Ӧ�����Ȼ�������H�Ľṹ��ʽ��F��Gֻ��1���Ȼ��������ѣ���Ӧ����̼̼˫�����ӵ��Ǹ��������ѣ�����Ӧi�ķ�Ӧ����ʽΪ ��NaOH
��NaOH ![]()
 ��CH3CH2OH��
��CH3CH2OH��
(5)���б������ܷ���ˮ�ⷴӦ������E�Ľṹ��ʽ������Ҫ���ͬ���칹���к���������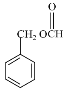 ��
�� ��
�� ���ڡ��䡢�����֣���
���ڡ��䡢�����֣��� ������6�֣���4��壬˵����4�ֲ�ͬ����ԭ�ӣ�����ԭ�Ӹ�����Ϊ3��2��2��1����������������
������6�֣���4��壬˵����4�ֲ�ͬ����ԭ�ӣ�����ԭ�Ӹ�����Ϊ3��2��2��1���������������� ��
�� ��
�� ��
��
(6)�������̣��Ʊ�![]() ����Ҫ��������
����Ҫ�������� ��C2H5COCCH2COOC2H5����������������D��E������Ʊ�
��C2H5COCCH2COOC2H5����������������D��E������Ʊ� ����Ҫ�ñ����ڼ�ȩ����ˮMg(OH)Cl���Ʊ����Ʊ�C2H5COCCH2COOC2H5����HOOCCH2COOH��C2H5OH��Ũ����������½��У����·����
����Ҫ�ñ����ڼ�ȩ����ˮMg(OH)Cl���Ʊ����Ʊ�C2H5COCCH2COOC2H5����HOOCCH2COOH��C2H5OH��Ũ����������½��У����·���� ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���õ������[CO(NH3)2]�ļ�����Һ��������װ����ͼ��ʾ������˵���������
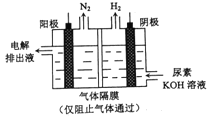
A. Ϊ��ǿ�����ԣ����ý���ͭ������
B. �����������������������������ʵ���֮��Ϊ3��1
C. �����ĵ缫��ӦʽΪ��2H2O+2e-=H2+2OH-
D. �����ĵ缫��ӦʽΪ��CO(NH2)2-6e-+8OH-=CO32-+N2+6H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��5-��ɫ���������Ǵ�Ѫ���з��ֵģ�����Ѫ���ء��㷺�����ڲ��鶯����֯�У���һ�����������ʡ������й�˵����ȷ����
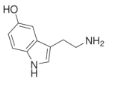
��֪����Ԫ���ӻ��ϵ�ԭ����ͬһƽ���ϡ�
A.һ����ƽ��� C ԭ���� 9 ��
B.�����ϵ�һ�ȴ����� 2 ��
C.�����к������ֹ����ţ��ɷ����ӳɡ���ȥ���к͵ȷ�Ӧ
D.5-��ɫ���ķ���ʽΪ C10H10N2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���G��![]() �������������ࡢ������������ǿ���������й���G��˵��������ǣ�������
�������������ࡢ������������ǿ���������й���G��˵��������ǣ�������
A.����ʽΪC11H14O
B.һ�ȴ�����8�֣������������칹��
C.����̼ԭ�ӿ�����ͬһƽ����
D.�ܷ���ȡ�����ӳɡ�������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ӵ���������ӵ�ؾ��и߰�ȫ�����������ͳɱ����ص㣬������Ϊ��һ����ء�ij�����ӵ�طŵ�ʱ���ܷ�ӦΪNa��1-x��MO2+NaxCn�TNaMO2+nC����ͼ��ʾ������̡��йظõ�ص�˵��������ǣ�������
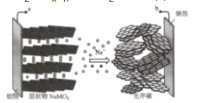
A.���ʱ��a����ӵ�Դ��������
B.�ŵ�ʱ�����·������b����a
C.���ʱ������̼�Ϸ����ķ�ӦΪnC+xNa++xe-�TNaxCn
D.�øõ�ص�⾫��ͭ���������Ǩ��1molNa+ʱ�������Ͽɻ��64g��ͭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������м��㣨ע�ⵥλ��
(1)�ڱ�״���£�1.7 g������ռ�����ԼΪ_________L������ͬ������_____mol H2S������ͬ����ԭ������
(2)�ڱ�״���£�0.5 mol�κ�����������ԼΪ________ L��
(3)4 g H2��22.4 L(��״��)CO2��ȣ�����������Ŀ�϶����________��
(4)0.01 molij���������Ϊ0.28 g���������Ħ������Ϊ________��
(5)0.3 mol NH3������������ԭ������____________��H2O������������ԭ������ȡ�
(6)��0.4 mol Al3����Al2(SO4)3��������SO![]() �����ʵ�����________mol��
�����ʵ�����________mol��
(7)2.3 g Na�к����ӵ����ʵ���Ϊ___________mol���ڸ�����ˮ��Ӧ��ʧȥ���ӵ����ʵ���Ϊ____________mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A.�����廯ʵ������Ҫ�������оƾ��ƣ�������ƿ�������ܣ���ƿ��
B.���غͼ�ȩ��һ���������ܷ�Ӧ���ɸ߷��Ӳ�����ȩ��֬
C.ú��������ָ������ú��ˮ�������õõ�CO��H2��CH4 ������
D.ʯ�͵ļӹ������У��д������ͼ����ѻ��ȹ��գ��������ǻ�÷���������Ҫ;��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijһ������ķ���ʽΪAB2��A����A��Ԫ�أ�B����A��Ԫ�أ�A��B��ͬһ���ڣ����ǵĵ縺��ֵ�ֱ�Ϊ3.44��3.98����֪AB2���ӵļ���Ϊ103.3���������ƶϲ���ȷ���ǣ� ��
A.AB2���ӵĿռ乹��Ϊ��V����
B.A---B��Ϊ���Թ��ۼ���AB2����Ϊ�Ǽ��Է���
C.AB2��H2O��ȣ�AB2���۵㡢�е��H2O�ĵ�
D.AB2����������ԭ�ӣ����Ӽ䲻���γ��������H2O���Ӽ����γ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״����Ҵ���Դ�ḻ���۸�������������淽�㣬������Ҫ�Ļ���ԭ�ϣ�������Ҫ����;��Ӧ��ǰ���������ö��ַ����ϳɡ�
I����CO2�����״����Ҵ�
(1)��֪��H2��ȼ����Ϊ-285.8 kJ/mol��CH3OH(l)��ȼ����Ϊ-725.8kJ/mol��CH3OH(g)=CH3OH(l) ��H= -37.3 kJ/mol����CO2(g)+3H2(g)=CH3OH(g)+ H2O(1) ��H=____kJ/mol��
(2)��CO2��H2�����ʵ���֮��1:3�������Ϊ2.0L�ĺ����ܱ������з�Ӧ[���� H2O(g)]����ͼ1��ʾѹǿΪ0.1 MPa��5.0 MPa��CO2ת�������¶ȵı仯��ϵ��

��a��b���㻯ѧ��Ӧ���ʷֱ���Va��Vb����ʾ����Va ___Vb������ڡ�����С�ڡ����ڡ�����
���г�a���Ӧ��ƽ�ⳣ������ʽK= ____________________��
(3)��1.0 L�����ܱ�������Ͷ��1 mol CO2��2.75 mol H2������Ӧ��CO2(g)+3H2(g) ![]() CH3OH (g)+H2O(g)��ʵ���ò�ͬ�¶ȼ�ѹǿ�£�ƽ��ʱ�״������ʵ����仯��ͼ2��ʾ������˵����ȷ����_____��
CH3OH (g)+H2O(g)��ʵ���ò�ͬ�¶ȼ�ѹǿ�£�ƽ��ʱ�״������ʵ����仯��ͼ2��ʾ������˵����ȷ����_____��
A.�÷�Ӧ������ӦΪ���ȷ�Ӧ
B��ѹǿ��С��ϵΪp1��p2��p3
C��M���Ӧ��ƽ�ⳣ��K��ֵԼΪ1.04��10��2
D����p2��512 Kʱ��ͼ��N����(��)����(��)
(4)CO2������ϳ��Ҵ��ķ�ӦΪ��2CO2(g)+6H2(g) ![]() C2H5OH(g) +3H2O(g) ��H��m������ʼʱ��Ͷ�ϱȣ���m��
C2H5OH(g) +3H2O(g) ��H��m������ʼʱ��Ͷ�ϱȣ���m��![]()

��ͼ3��Ͷ�ϱ���ͬ���¶�T3��T2��T1����÷�Ӧ���ʱ��H____0�������������������
��m=3ʱ���÷�Ӧ�ﵽƽ��״̬��p(��)=20a MPa����ѹ�����¸����ʵ����ʵ����������¶ȵĹ�ϵ��ͼ4��ʾ��������b����������Ϊ_________���ѧʽ����T4�¶�ʱ����Ӧ�ﵽƽ��ʱ����d�ķ�ѹp(d)=___________��
�״���Ӧ��
(5)�Լ״�Ϊ��Ҫԭ�ϣ��绯ѧ�ϳ�̼��������Ĺ���ԭ����ͼ5��ʾ��

���ӽ���ĤaΪ_____�����Ĥ��������Ĥ�����������ĵ缫��ӦʽΪ______________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com