


科目:高中化学 来源: 题型:
 (1)未用食用油炒咸菜的铁锅如果没有洗净,不久会出现红褐色锈斑.则铁锅的锈蚀属于
(1)未用食用油炒咸菜的铁锅如果没有洗净,不久会出现红褐色锈斑.则铁锅的锈蚀属于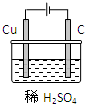

查看答案和解析>>
科目:高中化学 来源:2012-2013学年广东省陆丰市碣石中学高二上学期期末考试化学试卷(带解析) 题型:填空题
(1)用食用油炒咸菜的铁锅如果没有洗净,不久会出现红褐色锈斑。则铁锅的锈蚀属于 腐蚀(填“析氢”或“吸氧”);该腐蚀正极的电极反应式为 ;
此反应每转移2mol电子消耗的O2在标准状况下的体积为 L。
(2)某同学用碳棒、铜棒和稀硫酸为原材料,实现了在通常条件下不能发生的反应:Cu+H2SO4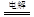 CuSO4+H2↑请在右边方框中画出能够实验这一反应的装置图(作必要的标注);某同学做该实验时,看到碳棒上有气泡产生,铜棒上气泡更多且没有被腐蚀,其原因是 。
CuSO4+H2↑请在右边方框中画出能够实验这一反应的装置图(作必要的标注);某同学做该实验时,看到碳棒上有气泡产生,铜棒上气泡更多且没有被腐蚀,其原因是 。
查看答案和解析>>
科目:高中化学 来源:2014届广东省陆丰市高二上学期期末考试化学试卷(解析版) 题型:填空题
(1)用食用油炒咸菜的铁锅如果没有洗净,不久会出现红褐色锈斑。则铁锅的锈蚀属于 腐蚀(填“析氢”或“吸氧”);该腐蚀正极的电极反应式为 ;
此反应每转移2mol电子消耗的O2在标准状况下的体积为 L。
(2)某同学用碳棒、铜棒和稀硫酸为原材料,实现了在通常条件下不能发生的反应:Cu+H2SO4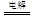 CuSO4+H2↑请在右边方框中画出能够实验这一反应的装置图(作必要的标注);某同学做该实验时,看到碳棒上有气泡产生,铜棒上气泡更多且没有被腐蚀,其原因是 。
CuSO4+H2↑请在右边方框中画出能够实验这一反应的装置图(作必要的标注);某同学做该实验时,看到碳棒上有气泡产生,铜棒上气泡更多且没有被腐蚀,其原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)未用食用油炒咸菜的铁锅如果没有洗净,不久会出现红褐色锈斑。则铁锅的锈蚀属于 腐蚀(填“析氢”或“吸氧”);该腐蚀正极的电极反应式为 ;此反应每转移2mol电子消耗的O2在标准状况下的体积为 L。
(2)某同学用碳棒、铜棒和稀硫酸为原材料,实现了在通
 常条件下不能发生的反应:Cu+H2SO4(稀)=CuSO4+H2↑。
常条件下不能发生的反应:Cu+H2SO4(稀)=CuSO4+H2↑。
请在右边方框中画出能够实验这一反应的装置图(作必
要的标注);某同学做该实验时,看到碳棒上有气泡产生,
铜棒上气泡更多且没有被腐蚀,其原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com