
| A. | Na2O2使有色物质褪色 | B. | 氯水使有色布条褪色 | ||
| C. | 活性炭使红墨水褪色 | D. | 漂白粉使某些染料褪色 |
分析 A、过氧化钠使有色物质褪色,是发生氧化还原漂白;
B、氯水使有色布条褪色,是氯气与水反应生成次氯酸;
C、活性炭使红墨水褪色,是活性炭的吸附性;
D、漂白粉使某些染料褪色,是漂白粉与二氧化碳与水反应生成次氯酸.
解答 解:A、过氧化钠使有色物质褪色,是发生氧化还原漂白,所以发生氧化还原反应,是化学变化,故A不选;
B、氯水使有色布条褪色,是氯气与水反应生成次氯酸,所以发生氧化还原反应,是化学变化,故B不选;
C、活性炭使红墨水褪色,是活性炭的吸附性,是物理变化,故C选;
D、漂白粉使某些染料褪色,是漂白粉与二氧化碳与水反应生成次氯酸,所以发生氧化还原反应,是化学变化,故D不选;
故选C.
点评 本题考查化学变化,学生只要知道化学变化的概念,观察有无新物质生成就可以迅速解题了,比较容易.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 由于电流的作用,酸、碱、盐溶于水发生电离 | |
| B. | 胶体的分散质粒子直径小于l00nm但大于1nm | |
| C. | 存在自由移动的离子是电解质溶液导电的原因 | |
| D. | 醋酸溶液中存在H+、CH3COOH、CH3COO-等微粒,故醋酸是弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用闻气味的方法鉴别氢气和氧气 | B. | 用氯化钡溶液鉴别盐酸和稀硫酸 | ||
| C. | 观察气体颜色区别氯气和氧气 | D. | 利用丁达尔效应区别溶液和胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
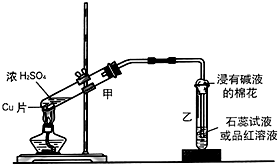 实验室常用下列装置来进行铜跟浓硫酸反应等一系列实验.
实验室常用下列装置来进行铜跟浓硫酸反应等一系列实验.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | PH=1的溶液中:Fe2+、NO3-、SO42-、Na+ | |
| B. | c(Fe3+)=0.1mol/L的溶液中:K+、ClO-、SO42-、SCN- | |
| C. | c(H+)/c(OH-)=1012的溶液中:NH4+、Al3+、NO3-、Cl- | |
| D. | 由水电离出的c(H+)=1×10-14mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同时改变两个变量来研究反应速率的变化,能更快得出有关规律 | |
| B. | 从HF、HCl、HBr、HI酸性递增的事实,推出F、Cl、Br、I的非金属递增的规律 | |
| C. | 决定化学反应速率的最主要因素:反应物自身的性质 | |
| D. | 依据丁达尔现象可将分散系分为溶液、胶体与浊液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
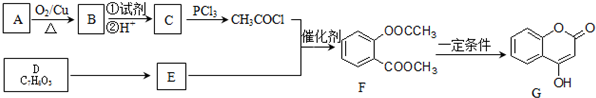
 .
.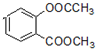 +3NaOH→CH3COONa+CH3OH+
+3NaOH→CH3COONa+CH3OH+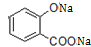 +H2O.
+H2O.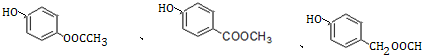 .
.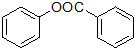 )是一种重要的有机合成中间体.试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任用).
)是一种重要的有机合成中间体.试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任用).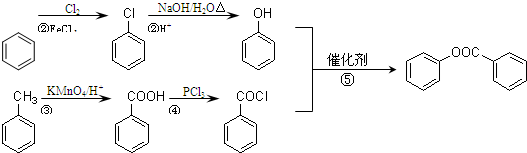
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 37.4g | B. | 44g | C. | 74.8g | D. | 88g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com