
【题目】用来表示可逆反应2A(g)+B(g)2C(g)(正反应为放热反应)的正确图象为( )
A.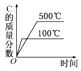
B.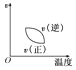
C.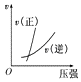
D.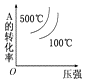
【答案】C
【解析】解:A.温度越高越先达平衡状态,500℃先达平衡;而且温度升高,反应向逆反应方向移动,C的质量分数减小,与图象符合,故A错误; B.升高温度,正逆反应速率都增大,与图象不符,故B错误;
C.反应物气体的计量数之和大于生成物,增大压强,平衡正向移动,正反应速率大于逆反应速率,故C正确;
D.增大压强,平衡正向移动,A的转化率增大,升高温度,平衡逆向移动,A的转化率减小,图象不符,故D错误.
故选C.
【考点精析】掌握化学平衡状态本质及特征是解答本题的根本,需要知道化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效).


科目:高中化学 来源: 题型:
【题目】
(1)已知:N2(g)+O2(g)=2NO(g) △H=+180.5kJ/mol
N2(g)+3H2(g) ![]() 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol
2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ/mol
写出氨气催化氧化生成一氧化氮气体和水蒸气的热化学反应方程式。
(2)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对N2(g)+3H2(g) ![]() 2NH3(g)反应的影响,实验结果如图所示:(图中T表示温度,n表示物质的量)
2NH3(g)反应的影响,实验结果如图所示:(图中T表示温度,n表示物质的量)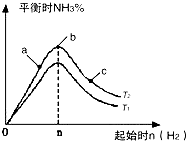
①图象中T2和T1的关系是:T2T1(填“高于”、“低于”、“等于”、“无法确定”).
②若比较在a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是(填字母).
(3)N2O5是一种新型硝化剂,其性质和制备受到人们的关注。一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g) ![]() 4NO2(g) + O2(g).△H﹥0,下表为反应在T1温度下的部分实验数据:
4NO2(g) + O2(g).△H﹥0,下表为反应在T1温度下的部分实验数据:
| 0 | 500 | 1000 |
| 5.00 | 3.52 | 2.48 |
①500s内NO2的平均生成速率为。
②该反应的化学平衡常数表达式为。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为元素周期表的一部分,其中X、Y、Z、W为四种短周期元素。Z元素原子核外K层与M层上的电子数相等。下列说法中正确的是( )
![]()
A. Y元素的最高价氧化物对应的水化物的化学式为H3YO4
B. Y的最简单气态氢化物的水溶液显弱碱性
C. 原子半径由小到大的顺序为X<Z<Y<W
D. X、Z两种元素的氧化物中所含化学键的类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.将BaSO4放入水中不能导电,所以硫酸钡不是电解质
B.NaCl溶液能导电,所以NaCl溶液是电解质
C.氯化氢溶于水能导电,所以盐酸是电解质
D.固态的NaCl不导电,熔融态NaCl可以导电
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了使K2S溶液中 ![]() 的比值变小,可加入的物质是( ) ①适量HCl(g)
的比值变小,可加入的物质是( ) ①适量HCl(g)
②适量NaOH(s)
③适量KOH(s)
④适量NaHS(s)
⑤适量的水.
A.②④
B.①②⑤
C.③④⑤
D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种短周期主族元素的原子序数依次增大,已知:
①其原子半径大小关系是D>E>B>C>A;
②A、D同主族,B、C、E分处三个连续的主族,且最外层电子数依次增加;
③C是地壳中含量最多的元素,D与C可形成原子个数比为1∶1或2∶1的化合物。
请填写以下空白:
(1)单质B的电子式为____________,结构式为____________。
(2)化合物D2C2的电子式为________________。用电子式表示D2C的形成过程:__________________________。
(3)单质A和单质B在一定条件下发生反应的化学方程式为_________________。
(4)单质E与A、C、D三种元素形成的化合物发生反应的化学方程式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列我国科学家中,为化学理论做出重大贡献的是
A. 徐光宪(创立稀土萃取理论) B. 屠呦呦(创制新的抗疟疾药)
C. 袁隆平(培育杂交水稻) D. 钱学森
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com