
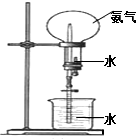
 如图所示,在干燥的圆底烧瓶里充满氨气,用带有玻璃管和滴管(滴管里预先吸入水)的塞子塞紧瓶口.立即倒置烧瓶,使玻璃管插入盛有水的烧杯里(预先在水里滴入少量酚酞溶液).打开橡皮管上的夹子,轻轻挤压滴管,使少量水进入烧瓶,可观察到的现象为:烧杯里的水由玻璃管进入烧瓶,形成喷泉,烧瓶内液体呈红色.
如图所示,在干燥的圆底烧瓶里充满氨气,用带有玻璃管和滴管(滴管里预先吸入水)的塞子塞紧瓶口.立即倒置烧瓶,使玻璃管插入盛有水的烧杯里(预先在水里滴入少量酚酞溶液).打开橡皮管上的夹子,轻轻挤压滴管,使少量水进入烧瓶,可观察到的现象为:烧杯里的水由玻璃管进入烧瓶,形成喷泉,烧瓶内液体呈红色.  阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | v(A)=0.5 mol•L-1•s-1 | B. | v(B)=0.3 mol•L-1•s-1 | ||
| C. | v(C)=0.6 mol•L-1•s-1 | D. | v(D)=1.6 mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 少量的钠保存在煤油中 | |
| B. | 铁粉要密封保存并置于干燥处 | |
| C. | 浓盐酸保存在密封玻璃瓶中 | |
| D. | 氢氧化钠溶液保存在玻璃塞的玻璃瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸馏、分液、萃取 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16O2和17O2都是氧的同素异形体 | |
| B. | 金属氧化物都是碱性氧化物 | |
| C. | 烟和雾可发生丁达尔现象,都属于胶体 | |
| D. | 合成纤维和光导纤维都是无机非金属材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3 C CO2 Ca(OH)2 HNO3 | B. | Na3PO4 Na SO2 H2SO3 KOH | ||
| C. | Si CO2 H3PO4 Ba(OH)2 Na2S | D. | N2 NO HNO3 NH3 NaBr |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
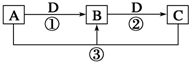 已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素.在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去).
已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素.在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com