
【题目】资源化利用CO具有重要意义。
(1)CO可设计成燃料电池,熔融Li2CO3和Na2CO3的混合物作为燃料电池的电解质,氧化剂是含CO2的O2,工作时正极反应为__________________,以该燃料电池为电源处理含氮氧化物废气,可回收硝酸,同时制得副产物氢气,装置如图所示(电极均为石墨电极)。该装置中应选用_______(填“阴”或“阳”)离子交换膜,写出电解时NO2发生反应的电极反应式:___________________。
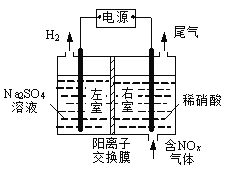
(2)CO是高炉炼铁的重要还原剂,炼铁时发生的主要反应有:
反应 | △H(kJ/mol) |
I. Fe2O3(s)+3C(s) | +489 |
II. Fe2O3(s)+3CO(g) | -27 |
III. C(s)+CO2(g) | X |
试计算,试计算,X=_________。
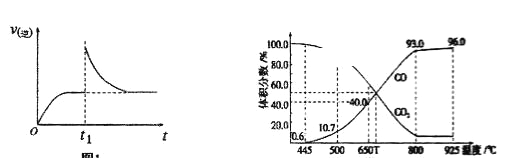
T1℃时,向某恒温密闭容器中加入一定量的Fe2O3和C,发生反应I,反应达到平衡后,在t1时刻改变某条件,v(逆)随时间(t)的变化关系如图所示,则t1时刻改变的条件可能是_____________________。
a.保持温度、体积不变,使用催化剂 b.保持体积不变,升高温度
c.保持温度不变,压缩容器体积 d.保持温度、体积不变,充入CO
(3)在一定温度下,向某体积可变的恒压(P总)密闭容器中加入1mol CO2与足量的碳发生反应III,平衡时体系中气体体积分数与温度的关系如图所示。
①650℃时,反应达平衡后CO2的转化率为____________。
②T℃时,该反应达到平衡时下列说法不正确的是__________________。
a.气体密度保持不变
b.2v正(CO2)=v正(CO)
c.若保持其它条件不变再充入等体积的CO2和CO,平衡向逆反应方向移动
d.若保持其它条件不变再充入惰性气体,v正、v逆均减小,平衡不移动
e.若其它条件不变将容器体积压缩至一半并维持体积不变,再次达平衡时压强小于原平衡的2倍
③根据图中数据,计算反应III在T℃时用平衡分压代替平衡浓度表示的化学平衡常数KP=___________(设总压强为P总,用含P总的代数式表示)
【答案】O2+2CO2+4e-=CO32- 阳 NO2 – e-+H2O=NO3-+2H+ +172 cd 25% cd 0.5 P总
【解析】
(1)在负极上CO放电,CO失电子结合CO32-生成CO2:CO-2e-+CO32-=2CO2;正极上CO2放电,CO2结合O2得到电子生成CO32-,电极反应式为:O2+2CO2+4e-=2CO32-;电解时,左室中电极上H+放电生成H2,则左室为阴极室,右室为阳极室,阳极上通入的是氮氧化物,生成的硝酸,阳极发生的反应为:NO2-e-+H2O=NO3-+2H+,右室中阳离子浓度增大,左室中水电离产生的H+放电,附近溶液的阳离子浓度降低,破坏了水的电离平衡,溶液中的阳离子由右室进入左室,所以离子交换膜为阳离子交换膜;
(2)( I-II)÷3可得:C(s)+CO2(g)![]() 2CO(g) △H=+172kJ/mol;
2CO(g) △H=+172kJ/mol;
a.保持温度、体积不变,使用催化剂,可以使正、逆反应速率都增大,但是平衡不发生移动,达到平衡时逆反应速率比原来的逆反应速率大,a错误;
b.保持体积不变,升高温度,正反应、逆反应速率增大,化学平衡常数改变,CO浓度不会回到原平衡状态,b错误;
c.保持温度不变,压缩容器体积,物质的浓度增大,反应速率加快,由于温度不变,所以化学平衡常数不变,CO决定化学平衡常数,最终CO浓度仍然回到原平衡状态,c正确;
d.保持温度、体积不变,充入CO,化学反应速率增大,不改变化学平衡常数,CO决定化学平衡常数,最终CO浓度仍然回到原平衡状态,d正确;
故合理选项是cd;
(3)①反应III为:C(s)+CO2(g)![]() 2CO(g)
2CO(g)
起始(mol) 1 0
转化(mol) x 2x
平衡(mol) 1-x 2x
![]() =60%,可得x=
=60%,可得x=![]() ,所以CO2的转化率为25%;
,所以CO2的转化率为25%;
②a.由于反应混合物不全为气体,所以若气体密度保持不变,则反应处于平衡状态,a正确;
b.由于方程式中CO2、CO的系数比为1:2,所以任何时刻都存在2v正(CO2)=v正(CO),b正确;
c.若保持其它条件不变再充入等体积的CO2和CO,相当于CO2增大的多,所以化学平衡向正反应方向移动,c错误;
d.若保持其它条件不变再充入惰性气体,由于物质的浓度不变,所以v正、v逆均不变,平衡不移动,d错误;
e.若其它条件不变将容器体积压缩至一半并维持体积不变,由于体积减小导致物质的浓度都增大,体系的压强增大,平衡向气体体积减小的逆反应方向移动,所以再次达平衡时压强小于原平衡的2倍,e正确;
故合理选项是cd;
③对于反应III,根据图中数据可知,在T℃时CO占总压强的![]() ,所以若用平衡分压代替平衡浓度表示的化学平衡常数KP=
,所以若用平衡分压代替平衡浓度表示的化学平衡常数KP=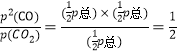 p(总)。
p(总)。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、N、W六种元素在周期表中的位置如图所示,下列说法不正确的是

A. 原子半径:r(Z)>r(M)>r(Y)
B. 最高价氧化物对应水化物酸性:M>N
C. N的单质能与Z和W形成的化合物发生置换反应
D. X能与另五种元素形成化合物,且X的化合价不完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的镁铝混合物投入200 mL硫酸中,固体全部溶解后,向所得溶液中加入5 mol/L的NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如图所示。
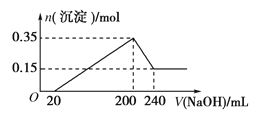
(1)加入NaOH 0~ 20mL 时发生反应离子方程式___________________,
加入NaOH 20~ 200mL 时发生反应离子方程式___________________,
加入NaOH 200~ 240mL 时发生反应离子方程式___________________,
(2)镁和铝的总质量为________g
(3)硫酸的物质的量浓度为___________ mol/L
(4)生成的氢气在标准状况下的体积为__________L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】简单原子的原子结构可用下图形象地表示:
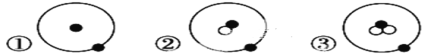
其中●表示质子或电子,○表示中子,则下列有关①②③的叙述正确的组合是( )
a.①②③互为同位素 b.①②③互为同素异形体
c.①②③是三种化学性质不同的粒子 d.①②③具有相同的质量数
e.①②③具有相同的质量 f.①②③是三种不同的原子
A. a、fB. d、eC. b、cD. e、f
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某密闭容器中加入 0.3 mol A、0.1 mol C 和一定量的 B 三种气体, 一定条件下发生如下反应: 3A(g) ![]() B(g)+2C(g),各物质的浓度随时间变化如图所示[t0~t1 阶段的 c(B)变化未画出]。下列说法中正确的是( )
B(g)+2C(g),各物质的浓度随时间变化如图所示[t0~t1 阶段的 c(B)变化未画出]。下列说法中正确的是( )

A. 若 t1=15 s,则用 A 的浓度变化表示 t0~t1阶段的平均反应速率为 0.004 mol·L-1·s-1
B. t1时该反应达到平衡, A 的转化率为 60%
C. 该容器的容积为2 L,B的起始的物质的量为 0.02 mol
D. t0~t1 阶段, 此过程中容器与外界的热交换总量为 a kJ,该反应的热化学方程式为 3A(g)![]() B(g)+2C(g) ΔH=-50a kJ·mol-1
B(g)+2C(g) ΔH=-50a kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应A (g)+ 3B(g) =2C(g) + 2D(g),下列数据表示反应进行得最快的是( )
A. v(A)=0.7mol/(L·s)B. v (B) =1.8mol/(L· s)
C. v (C)=1mol/(L·s)D. v (D) =1.6mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NaHSO4在水中的电离方程式为NaHSO4===Na++H++SO42-。某温度下,向c(H+)=1×10-6 mol·L-1的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的c(H+)=1×10-2 mol·L-1。下列对该溶液的叙述不正确的是
A. 该温度高于25℃
B. 由水电离出来的H+的浓度为1×10-10 mol·L-1
C. 加入NaHSO4晶体抑制了水的电离
D. 取该溶液加水稀释100倍,溶液中的c(OH-)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭恒容容器中,加入1molN2和3molH2发生反应:N2(g)+3H2(g)2NH3(g),下列叙述中能说明该反应达到平衡状态的是( )
A.![]() B.混合气体的密度保持不变
B.混合气体的密度保持不变
C.混合气体的平均相对分子质量保持不变D.![]() :
:![]() :
:![]() :3:2
:3:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com