
某含氯化合物A由两种短周期元素组成,常温下该物质为气态,测得该气体对空气的相对密度为3.0,A溶于水可得只含单一溶质B的弱酸性溶液,B溶液在放置过程中其酸性会增强。常温下,气体A与NH3反应生成离子晶体C、气体单质D和常见液体E,D为空气中含量最多的物质。气体A可用某一气体单质与潮湿的Na2CO3 反应制得,同时生成两种钠盐。请回答下列问题:
(1)气体A的化学式为 ,气体单质D对应元素在周期表中的位置为 。
(2)用化学方程式表示B溶液酸性增强的原因 。
(3)气体A与NH3反应的化学方程式为 ,该反应体现气体A具有 性。
(4)试写出制取气体A的化学方程式为 。
(5)设计实验探究离子晶体C的成分为 。
 得只含单一溶质B的弱酸性溶液,B溶液在放置过程中其酸性会增强,所以B是次氯酸。常温下,气体A与NH3反应生成离子晶体C、气体单质D和常见液体E,D为空气中含量最多的物质,则D是氮气。这说明该反应中氨气被氧化生成氮气,而还原产物是氯化氢,进而与氨气反应生成氯化铵,即C是氯化铵。根据原子守恒可知,E是水。气体A可用某一气体单质与潮湿的Na2CO3 反应制得,同时生成两种钠盐。因此根据原子守恒可知,该气体应该是氯气,反应的方程式为2Cl2+2Na2CO3+H2O=Cl2O+2NaHCO3+2NaCl。
得只含单一溶质B的弱酸性溶液,B溶液在放置过程中其酸性会增强,所以B是次氯酸。常温下,气体A与NH3反应生成离子晶体C、气体单质D和常见液体E,D为空气中含量最多的物质,则D是氮气。这说明该反应中氨气被氧化生成氮气,而还原产物是氯化氢,进而与氨气反应生成氯化铵,即C是氯化铵。根据原子守恒可知,E是水。气体A可用某一气体单质与潮湿的Na2CO3 反应制得,同时生成两种钠盐。因此根据原子守恒可知,该气体应该是氯气,反应的方程式为2Cl2+2Na2CO3+H2O=Cl2O+2NaHCO3+2NaCl。
(1)气体A的化学式为Cl2O,气体单质D对应元素氮元素在周期表中的位置为第二周期第ⅤA族。
(2)次氯酸不稳定,受热易分解,生成氯化氢和氧气,因此溶液的酸性增强,反应的化学方程式为2HClO=2HCl + O2 ↑。

考点:考查物质推断、元素周期表的结构、氧化还原反应的有关判断与应用以及离子的检验


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既不是氧化剂又不是还原剂等。下列反应与Br2 + SO2 + 2H2O H2SO4 + 2HBr相比较,水的作用不相同的是
A.2Na2O2 + 2H2O 4NaOH + O2↑ B.4Fe(OH)2 + O2 + 2H2O 4Fe(OH)3
C.2F2 + 2H2O 4HF + O2 D.C12 + H2O HC1 + HC1O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列做法中不正确的是
A.向污水中加入适量明矾,可除去其中的悬浮物
B.用氢氟酸刻蚀工艺玻璃上的纹饰
C.从碘水中提取单质碘时,可用无水乙醇代替CCl4
D.在海轮外壳上嵌入锌块,可减缓船体的腐蚀速率
查看答案和解析>>
科目:高中化学 来源: 题型:
常温常压时,下列叙述不正确的是( )
A. pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(Na2CO3)<c(CH3COONa)
B.pH=5的①NH4Cl溶液②CH3COOH溶液③稀盐酸溶液中c(H+)水:①>②>③
C.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色
D.0.1 mol/L的醋酸的pH =a,0.01mol/L的醋酸的pH =b,则b<a+l
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示表示阿伏伽德罗常数的值,下列说法正确的是
A.1mol Na2O2粉末中含离子总数为4NA
B.22.4LCO2中含有的原子数为3NA
C.1mol单质钠在常温下或点燃条件下与O2完全反应转移的电子数都为NA
D.在一定量的稀硝酸中加入56g铁粉且完全溶解,转移的电子一定为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
相同碳原子数的烷烃、烯烃、炔烃,在空气中完全燃烧生成二氧化碳和水,需要空气量的比较中正确是 ( )
A.烷烃最多 B.烯烃最多 C.炔烃最多 D.三者一样多
查看答案和解析>>
科目:高中化学 来源: 题型:
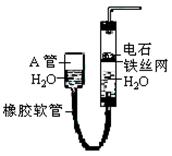 |
右图中的实验装置可用于制取乙炔,请填空:
(1)图中,A管的作用是 ;
制取乙炔的化学方程式是 ;
(2)乙炔通入KMnO4酸性溶液中观察到的现象是
乙炔发生了 反应;
(3)乙炔通入溴的CCl4溶液中观察到的现象是 ,
乙炔发生了 反应
查看答案和解析>>
科目:高中化学 来源: 题型:
在实验室中,对下列事故或药品的处理正确的是
A. 金属钠着火燃烧时,用泡沫灭火器灭火
B.有氯气泄漏时,用肥皂水浸湿软布蒙面,并迅速离开现场
C.少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗
D.含硫酸的废液倒入水槽,用水冲入下水道
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com