
将铜棒和锌棒用导线连接后插入稀硫酸溶液中,下列叙述中正确的是( )
A.该装置能形成原电池,其中锌是负极 B.该装置能形成原电池,其中铜是负极
C.该装置不能形成原电池 D.以上说法均不正确
 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源:2016届安徽省六安市高三下综合训练十理综化学试卷(解析版) 题型:实验题
高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,不会造成二次污染。
己知高铁酸盐热稳定性差,工业上用湿法制备高铁酸钾的基本流程如下图所示:
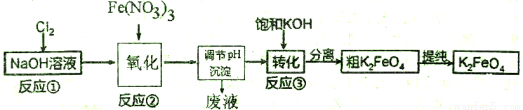
(1)①上述氧化过程中,发生反应的离子方程式是__________,在实际生产中一般控制反应温度30℃以下,其原因是__________。
②沉淀过程中加入浓KOH溶液可析出高铁酸钾(K2FeO4 ),这说明__________。
③在提纯K2FeO4中采用重结晶、洗涤、低温烘干的方法,沉淀洗涤方法是__________。
④某温度下,将C12通入NaOH溶液中,反应后得到NaCl,NaC1O,NaClO3的混合溶液,经测定ClO-与C1O3-离子的物质的量之比是1: 2,则C12与氢氧化钠反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为__________。
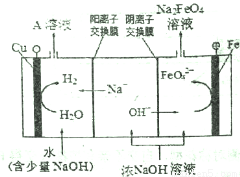
(2)工业上还可用通过电解浓NaOH溶液制备Na2FeO4,其工作原理如下图所示:阳极的电极反应式为__________,其中可循环使用的物质是__________。
(3)CO2可转化为碳酸盐,其中Na2CO3是一种用途广泛的碳酸盐.己知:25℃时,几种酸的电离平衡常数如下表所示。

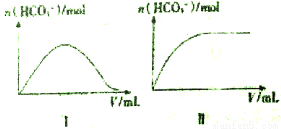
25℃时,向一定浓度的Na2CO3溶液中分别滴入等物质的量浓度的下列溶液至过量:
①NaHSO3②HNO3③HC1O,溶液中的n (HCO3-)与所加入溶液体积(V)的关系如上图所示。其中符合曲线Ⅱ的溶液为__________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二下期中化学试卷(解析版) 题型:填空题
研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题:
(1)C、Si、N的电负性由大到小的顺序是 。C60和金刚石都是碳的同素异形体,二者比较,熔点高的是 。
(2)A、B均为短周期金属元素,依据下表数据,写出B的基态原子的电子排布式 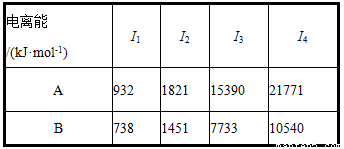
过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般地,为d0或d10排布时,无颜色,为d1~d9排布时,有颜色。如[Co(H2O)6]2+显粉红色。据此判断,
[Mn(H2O)6]2+ (填“无”或“有”)颜色。
(4)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等。
①每个COCl2分子内含有 个σ键, 个π键。其中心原子采取 杂化轨道方式。
②配合物Fe(CO)5的配体是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二下期中化学试卷(解析版) 题型:选择题
某元素X的逐级电离能如图所示,下列说法正确的是( )
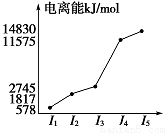
A.X元素显+4价
B.X为非金属
C.X为第五周期元素
D.X与氯反应时最可能生成的阳离子为X3+
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃会宁一中高一下期中文科化学试卷(解析版) 题型:选择题
(1)碱金属元素原子的最外层电子都是 个,在化学反应中它们容易失去 个电子;碱金属元素中金属性最强的是 ,原子半径最小的是 。卤族原子的最外层电子都是 个,在化学反应中它们容易得到 个电子;卤族元素中非金属性最强的是 ,原子半径最小的是 。
(2)元素周期表的第三周期元素,从左到右,原子半径逐渐_____________ ;元素的金属性逐渐_____________ ,非金属性逐渐_____________ 。该周期元素中,除稀有气体外,原子半径最大的是_____________ ;最高价氧化物对应水化物碱性最强的是_____________ ;最高价氧化物对应水化物呈两性的是_____________ 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃会宁一中高一下期中文科化学试卷(解析版) 题型:选择题
在元素周期表中金属元素与非金属元素的分界线附近的一些元素能用于制( )
A.合金 B.半导体 C.催化剂 D.农药
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃会宁一中高一下期中理科化学试卷(解析版) 题型:实验题
某同学设计如下三个实验方案以探究某反应是放热反应还是吸热反应:
方案一:如图1,在小烧杯里放一些除去氧化铝保护膜的铝片,然后向烧杯里加入10 mL 2 mol·L-1稀硫酸,再插入一支温度计,温度计的温度由20 ℃逐渐升至75 ℃,随后,温度逐渐下降至30 ℃,最终停留在20 ℃。
方案二:如图2,在烧杯底部用熔融的蜡烛粘一块小木片,在烧杯里加入10 mL 2 mol·L-1硫酸溶液,再向其中加
入氢氧化钠溶液,片刻后提起烧杯,发现小木片脱落下来。
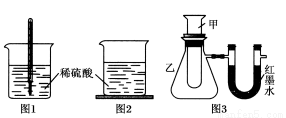
方案三:如图3,甲试管中发生某化学反应,实验前U形管红墨水液面相平,在化学反应过程中,通过U形管两侧红
墨水液面高低判断某反应是吸热反应还是放热反应。
序号 | 甲试管里发生反应的物质 | U形管里红墨水液面 |
① | 氧化钙与水 | 左低右高 |
② | 氢氧化钡晶体与氯化铵晶体(充分搅拌) | ? |
③ | 铝片与烧碱溶液 | 左低右高 |
④ | 铜与浓硝酸 | 左低右高 |
根据上述实验回答相关问题:
(1)铝片与稀硫酸的反应是________(填“吸热”或“放热”)反应,写 出该反应的离子方程式:___________。
(2)方案一中,温度升至最大值后又下降的原因是___________。
(3)方案二中,小木片脱落的原因是________,由此得出的结论是__________________。
(4)方案三中,如果甲试管里发生的反应是放热反应,则U形管里红墨水液面:左边________(填“高于”“低于”或“等于”)右边。
(5)由方案三的现象得出结论:①③④组物质发生的反应都是________(填“吸热”或“放热”)反应,如果放置较长时间,可观察到U形管里的现象是______________。
(6)方案三实验②的U形管中的现象为________,说明反应物的总能量________(填“大于”“小于”或“等于”)生成物的总能量
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃会宁一中高一下期中理科化学试卷(解析版) 题型:选择题
在元素周期表中金属与非金属的分界处,可以找到 ( )
A.合金 B.半导体材料 C.催化剂 D.农药
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高一下学期期末化学试卷(解析版) 题型:选择题
通常用来衡量一个国家石油化学工业发展水平的标志是( )
A、合成纤维的产量 B、硫酸的年产量
C、乙烯的年产量 D、石油的年产量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com