
| A、-OH |
| B、-COOH |
| C、-C6H5 |
| D、-NH2 |
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:

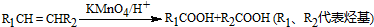

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、①②③④ |
| C、②③ | D、③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只要溶液里有H+,溶液就显酸性 |
| B、H+浓度增大,溶液的酸性一定增强 |
| C、c(H+)>c(OH-),溶液一定显酸性 |
| D、强酸溶液的酸性一定比弱酸溶液的酸性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
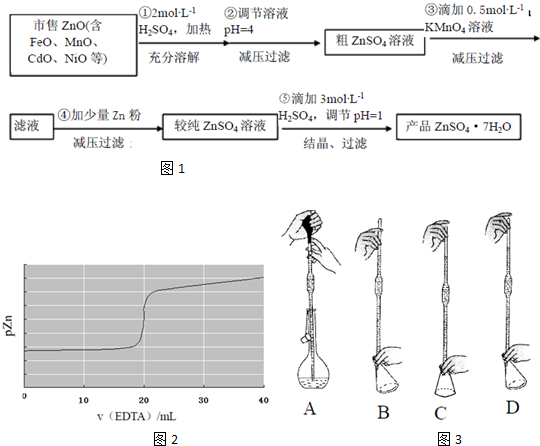
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知Ⅰ.N-N键键能为167kJ?mol-1,N≡N键键能为942kJ?mol-1,
已知Ⅰ.N-N键键能为167kJ?mol-1,N≡N键键能为942kJ?mol-1,| A、+1066.4 kJ?mol-1 |
| B、-1066.4 kJ?mol-1 |
| C、+697.6 kJ?mol-1 |
| D、-697.6 kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Fe3+、Cl-、SO32- |
| B、K+、Na+、SO42-、NO3- |
| C、Na+、Cu2+、S2-、NO3- |
| D、Al3+、K+、HCO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 用活性炭还原法处理氮氧化物.有关反应为:C(s)+2NO(g)?N2 (g)+CO2 (g).某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
用活性炭还原法处理氮氧化物.有关反应为:C(s)+2NO(g)?N2 (g)+CO2 (g).某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:浓度/mol?L-1 时间/min | NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 10 | 0.58 | 0.21 | 0.21 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com