
| A. | 降低压强能加快化学反应速率 | |
| B. | 使用适当催化剂可以加快化学反应速率 | |
| C. | 升高温度能加快化学反应速率 | |
| D. | 增大压强可以加快此反应的速率 |
分析 影响反应速率的因素主要有温度、压强、浓度、催化剂、表面积等,升高温度会加快反应速率;对有气体参加的反应,增大压强会增大反应速率;增大浓度会增大反应速率;使用催化剂可以加快反应速率,以此解答该题.
解答 解:A.对于有气体参加的化学反应,降低压强,化学反应速率减慢,故A错误;
B.催化剂能改变反应的活化能,加入催化剂能改变反应速率,可以加快化学反应速率,故B正确;
C.温度对任何化学反应的速率都会造成影响,升高温度,反应速率变大,故C正确;
D.对于有气体参加的化学反应,压强会对反应速率造成影响,增大压强,浓度增大,反应速率增大,故D正确.
故选A.
点评 本题主要考查化学反应速率的影响因素,为高频考点,侧重于学生的分析能力的考查,难度不大,题目难度不大,从温度、压强、催化剂对反应速率的影响是解题的突破口.


科目:高中化学 来源: 题型:选择题
| A. | 丙烯能发生加成反应,而丙烷不能发生加成反应 | |
| B. | 甲苯能使酸性高锰酸钾溶液褪色,而苯不能使酸性高锰酸钾溶液褪色 | |
| C. | 乙烯能使酸性高锰酸钾溶液褪色,而聚乙烯不能 | |
| D. | 烃类物质都能燃烧生成二氧化碳和水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 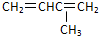 3-甲基-1,3-丁二烯 3-甲基-1,3-丁二烯 | B. | CH3CH(OH)CH2CH32-羟基丁烷 | ||
| C. |  顺-2-丁烯 顺-2-丁烯 | D. | CH3CH(NH2)CH2COOH 3-氨基丁酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 在相同条件下,将等量的硫蒸气和硫固体分别完全燃烧,前者放出热量多 | |
| B. | 由 C(s,石墨)→C(s,金刚石)-1.9kJ可知,金刚石比石墨稳定 | |
| C. | 在稀溶液中:H+(aq)+OH-(aq)→H2O(l)+57.3kJ,若将含0.5mol H2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量大于57.3 kJ | |
| D. | 在101kPa时,2g H2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式可表示为:2H2(g)+O2(g)→2H2O(l)+285.8kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠的金属性比钾强,工业上用钠制取钾(Na+KCl $\frac{\underline{\;800℃\;}}{\;}$K↑+NaCl) | |
| B. | 利用Al2O3制作的坩埚,可用于熔融烧碱 | |
| C. | 氢氟酸具有强酸性,用氢氟酸蚀刻玻璃 | |
| D. | 制水泥和玻璃都用石灰石作原料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca:1s22s22p63s23p63d2 | B. | Cu:3d94s2 | ||
| C. | Fe:3d64s2 | D. | C:1s22s12p3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com