
研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1)已知:2SO2(g)+O2(g)  2SO3(g) ΔH= -196.6kJ·mol-1
2SO3(g) ΔH= -196.6kJ·mol-1
2NO(g)+O2(g)  2NO2(g) ΔH= -113.0kJ·mol-1
2NO2(g) ΔH= -113.0kJ·mol-1
则反应NO2(g)+SO2(g)  SO3(g)+NO(g)的ΔH= kJ·mol-1
SO3(g)+NO(g)的ΔH= kJ·mol-1
(2)一定条件下,将NO2与SO2以体积比2∶1置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
A.体系压强保持不变
B.混合气体颜色保持不变
C.SO3和NO的体积比保持不变
D.每消耗1molSO3的同时生成1mol NO
测得上述反应达平衡时NO2与SO2的体积比为5∶1,则平衡常数K=
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)  CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图(2)所示。该反应ΔH 0(填“>”或“<”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是: 。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图(2)所示。该反应ΔH 0(填“>”或“<”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是: 。
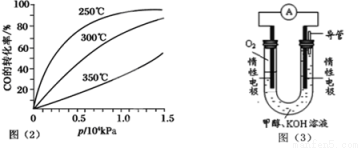
(4)依据燃烧的反应原理,合成的甲醇可以设计如图(3)所示的原电池装置。
①该电池工作时,OH-向 极移动(填“正”或“负”)。
②该电池正极的电极反应式为 。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015-2016学年福建省高一下学期期末化学试卷(解析版) 题型:填空题
下表是元素周期表的一部分,表中的每个字母表示一种短周期元素,回答下列问题:
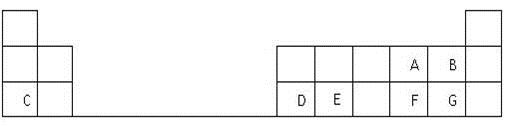
(1)G在元素周期表中的位置是 。
(2)A、B、C三种元素的简单离子半径由大到小的顺序为 (用离子符号表示)。
(3)写出C和F两种元素形成的化合物的电子式 ,
(4)元素E是构成地壳的主要元素之一,其氧化物是制光导纤维的基本原料,该氧化物中含有的化学键是 键(填“离子”或“共价”),属于 晶体(填晶体类型),写出该氧化物与C元素最高价氧化物水化物反应的离子方程式 。
(5)C离子的氧化性比D离子的氧化性 ,(填“强”或“弱”),其原因是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二下学期第四次月考化学试卷(解析版) 题型:选择题
下列有关物质的分离或提纯的说法中正确的是( )
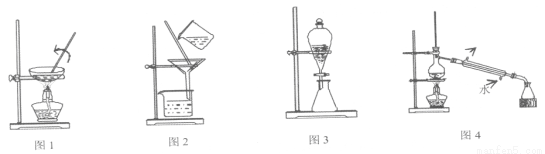
A.图①:从FeCl2溶液中制取FeCl2晶体
B.图②:从制取Fe(OH)3胶体的混合物中提纯胶体
C.图③:用CCl4萃取,从溴水中得到纯溴
D.图④:分离苯和甲苯
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省邯郸市高二下学期期末化学试卷(解析版) 题型:选择题
向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液。下列对此现象说法正确的是 ( )
A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变。
B.沉淀溶解后,将生成深蓝色的配合离子[Cu(NH3)4] 2+。
C.向反应后的溶液加入乙醇,溶液没有发生变化 。
D.在[Cu(NH3)4] 2+离子中,Cu2+给出孤对电子,NH3提供空轨道。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省邯郸市高二下学期期末化学试卷(解析版) 题型:选择题
下列分子或离子中,中心原子含有孤对电子的是
A.NH4+ B.CCl4 C.SiH4 D.H3P
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省厦门市高一下学期期末化学试卷(解析版) 题型:选择题
己知反应A(g)+B(g)  C(g)+D(g)的平衡常数K值与温度的关系如下表所示.830℃时,向一个2L的密闭容器中充入0.20molA和0.80molB,4s内v(A)=0.005 mol·L-1·S-1.
C(g)+D(g)的平衡常数K值与温度的关系如下表所示.830℃时,向一个2L的密闭容器中充入0.20molA和0.80molB,4s内v(A)=0.005 mol·L-1·S-1.
下列说法正确的是( )
温度/℃ | 700 | 830 | 1200 |
K值 | 1.7 | 1.0 | 0.4 |
A.4s时,c(B)为0.76 mol·L-1
B. 830℃到平衡时,A的转化率为80%
C. 达平衡时,升高温度,平衡正向移动
D.1200 ℃时反应C(g)+D(g)  A(g)+B(g)的平衡常数的值为0.4
A(g)+B(g)的平衡常数的值为0.4
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省厦门市高一下学期期末化学试卷(解析版) 题型:选择题
一定条件下,制备特种陶瓷的原料MgO:MgSO4(s)+CO(g)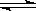 MgO(s)+CO2(g)+SO2(g)ΔH>0。该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是( )
MgO(s)+CO2(g)+SO2(g)ΔH>0。该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是( )
选项 | x | y |
|
A | 温度 | 容器内混合气体的密度 | |
B | CO的物质的量 | CO2与CO的物质的量之比 | |
C | SO2的浓度 | 平衡常数K | |
D | MgSO4的质量(忽略体积) | CO的转化率 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省厦门市高二下学期期末化学试卷(解析版) 题型:填空题
FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小,请回答下列问题:
(1)FeCl3净水的原理是_________________;
(2)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3。若酸性FeCl2废液中c(Fe2+)=2.0×10-2mol•L-1,c(Fe3+)=1.0×10-3mol•L-1,c(Cl-)=5.3×10-2mol•L-1,则该溶液的pH约为_________________;
(3)FeCl3在溶液中分三步水【解析】
Fe3++H2O Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O Fe(OH)2++H+ K2
Fe(OH)2++H+ K2
Fe(OH)2++H2O Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
以上水解反应的平衡常数K1、K2、K3由大到小的顺序是_________________;
(4)通过控制条件,以上水解产物聚合,生成聚合氯化铁,离子方程式为:xFe3++yH2O?Fex(OH)y(3x-y)++yH+,欲使平衡正向移动可采用的方法是(填序号)_________________
a.降温 b.加水稀释 c.加入NH4Cl d.加入NaHCO3
(5)室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条是_________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省洞口县高二下学期期末化学试卷(解析版) 题型:选择题
下列图中的实验方案,能达到实验目的的是
A | B | C | D | |
实验方案 |
|
|
|
|
实验 目的 | 验证FeCl3对H2O2分解反应有催化作用 | 制备Fe(OH)2并能较长时间观察其颜色 | 除去CO2气体中混有的SO2 | 比较HCl、H2CO3和H2SiO3的酸性强弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com