
| A. | CH3CH2CHBrCH2Br | B. | CH3CHBrCHBrCH3 | C. | 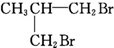 | D. |  |
分析 CH2═CH-CH2-CH3与Br2加成反应是不饱和碳原子上分别连接一个溴原子,断裂碳碳双键中的一个化学键,形成卤代烃,据此分析判断.
解答 解:CH2═CH-CH2-CH3,是1-丁烯,和Br2发生加成反应,不饱和碳原子上分别连接一个溴原子,断裂1、2号碳原子间双键上的一个共价键形成的化合物,CH2═CH-CH2-CH3+Br-Br→CH3CH2CHBrCH2Br,
A.结构简式符合,故A正确;
B.双键位置不对,得到CH3CHBrCHBrCH3产物的烯烃为:CH3-CH=CH-CH3,故B错误;
C.溴原子的位置不符合加成反应特征,故C错误;
D.双键位置不对,得到 产物的烯烃结构简式为(CH3)2C=CH2,不是由CH2═CH-CH2-CH3与Br2加成得到,故D错误;
产物的烯烃结构简式为(CH3)2C=CH2,不是由CH2═CH-CH2-CH3与Br2加成得到,故D错误;
故选A.
点评 本题考查了烯烃加成反应的特征分析判断,掌握加成原理是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 该反应中Al是还原剂,稀硫酸是氧化剂 | |
| B. | 该反应中消耗Al的质量为1.8g | |
| C. | 生成2.24L H2 | |
| D. | 该反应中有0.3NA个电子发生转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔是国际单位制的七个物理量之一 | |
| B. | 摩尔是表示物质质量的单位 | |
| C. | 科学上规定含有阿伏加德罗常数个粒子的任何粒子集合体为1mol | |
| D. | 1mol氧含6.02×1023个O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
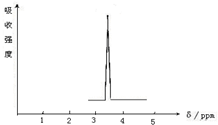 按要求完成下列问题:
按要求完成下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质的沸点:Z>X | |
| B. | 原子序数:Z>X>W | |
| C. | 原子的最外层电子数:Y>W>Z | |
| D. | 标准状况下,5.6LW的单质中含有0.5mol原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该元素最高价氧化物的水化物肯定是一种强酸 | |
| B. | 该元素单质肯定是一种黄绿色的气体 | |
| C. | 该元素的最高价氧化物肯定能与强碱反应 | |
| D. | 该元素的原子半径在同周期中肯定是最小的(稀有气体元素除外) |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

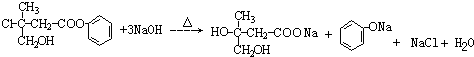 .
.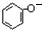 +CO2+H2O→
+CO2+H2O→ +HCO3-.
+HCO3-. .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
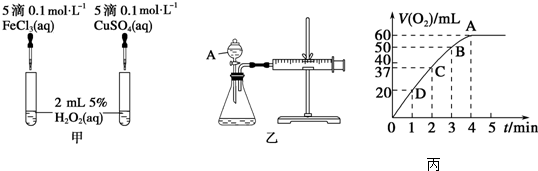
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1mol任何气体都含有相同的原子数 | |
| B. | 在100℃、1×104Pa时,1mol O2中约含有6.02×1023个O2分子 | |
| C. | 含有阿伏加德罗常数个水分子的水(4℃)其体积为18mL(ρ=1g/cm3) | |
| D. | 两种物质完全反应时,它们的物质的量一定相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com