
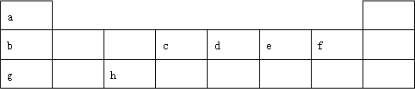
 ,故答案为:
,故答案为: ;
;

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、某溶液中滴加AgNO3溶液有白色沉淀,说明原溶液中有Cl- |
| B、某溶液中先滴加足量盐酸无现象,再滴加BaCl2溶液有白色沉淀,说明原溶液中有SO42- |
| C、某溶液中滴加NaOH溶液有蓝色沉淀,说明原溶液中有Cu2+ |
| D、某溶液中滴加稀硫酸生成无色气体,说明原溶液中有CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
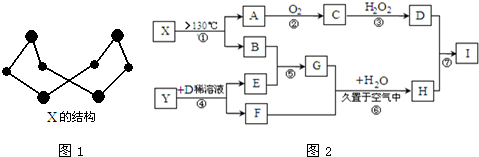
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
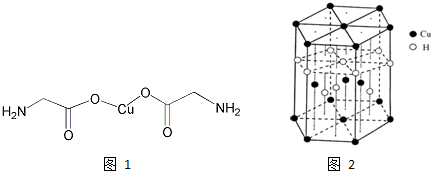
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、大量排放SO2、NO2或CO2都会导致酸雨的形成 |
| B、利用太阳能、潮汐能、风力发电,以获取清洁能源 |
| C、采用纳米二氧化钛光触媒技术.将汽车尾气中的NO和CO转化为无害气体 |
| D、在家用燃煤中加人适量的生石灰能有效减少二氧化硫的排放量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com