
【题目】![]() 时,用浓度为
时,用浓度为![]() 的NaOH溶液滴定
的NaOH溶液滴定![]() 浓度均为
浓度均为![]() 的三种酸HX、HY、HZ,滴定曲线如图所示.下列说法正确的是
的三种酸HX、HY、HZ,滴定曲线如图所示.下列说法正确的是![]()

A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:![]()
B.用NaOH溶液滴定HY,当![]() 时溶液中
时溶液中![]()
C.用NaOH溶液滴定HY,当![]() 时溶液中
时溶液中![]()
D.当三种酸均滴定至![]() 时,HZ所用NaOH溶液体积最小
时,HZ所用NaOH溶液体积最小
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.![]() 的一溴代物和CH3CH(CH3)CH2CH3的一溴代物都有4种(不考虑立体异构)
的一溴代物和CH3CH(CH3)CH2CH3的一溴代物都有4种(不考虑立体异构)
B.![]() 与
与![]() 互为同系物
互为同系物
C.按系统命名法,化合物![]() 的名称是2,3,4-三甲基-2-乙基戊烷
的名称是2,3,4-三甲基-2-乙基戊烷
D.CH3CH(CH3)CH2CH3分子中的四个碳原子在同一直线上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图与对应的叙述相符的是![]()
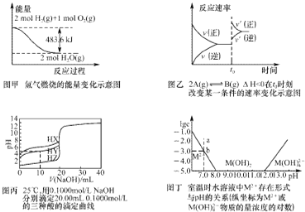
A.由图甲可知:![]() 的燃烧热为
的燃烧热为![]()
B.由图乙可知:![]() 时刻改变的条件是增大压强或者升高温度
时刻改变的条件是增大压强或者升高温度
C.由图丙可知:将上述HX、HY、HZ溶液等体积混合,用NaOH溶液滴定至HX恰好完全反应时,溶液中的离子浓度:![]()
D.由图丁可知:室温时![]() 的溶度积常数为
的溶度积常数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是

A.图①中△H1=△H2+△H3
B.图②在催化剂条件下,反应的活化能等于E1+E2
C.图③表示醋酸溶液滴定 NaOH 和氨水混合溶液的电导率变化曲线
D.图④可表示由CO(g)生成CO2(g)的反应过程和能量关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学中常用图像直观的描述化学反应的进程或结果。下列图像描述正确的是:
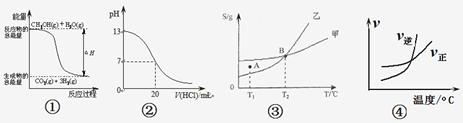
A.根据图①可判断反应CH3OH(g)+H2O(g)=CO2(g)+3H2(g)的ΔH<0
B.图②表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1NaOH溶液的pH随加入酸体积的变化
C.根据图③(S表示溶解度),A点表示T1℃时甲为饱和溶液,乙溶液未饱和。
D.根据图④可判断可逆反应A2(g)+3B2(g)![]() 2AB3(g)的ΔH>0
2AB3(g)的ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物![]() (
(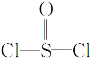 )是一种液态化合物,沸点77 ℃,在盛有
)是一种液态化合物,沸点77 ℃,在盛有![]() 水的锥形瓶中小心地滴加8~10滴
水的锥形瓶中小心地滴加8~10滴![]() ,可观察到反应剧烈,液面上有白雾形成,并逸出有气味的气体,该气体可使沾有品红试液的滤纸褪色。轻轻振荡锥形瓶,待白雾消失后往溶液中滴加
,可观察到反应剧烈,液面上有白雾形成,并逸出有气味的气体,该气体可使沾有品红试液的滤纸褪色。轻轻振荡锥形瓶,待白雾消失后往溶液中滴加![]() 溶液,有不溶于稀硝酸的白色沉淀析出。
溶液,有不溶于稀硝酸的白色沉淀析出。
(1)根据以上实验,写出![]() 与水反应的化学方程式:_____________________________________。
与水反应的化学方程式:_____________________________________。
(2)蒸干![]() 溶液得不到
溶液得不到![]() 固体,只能得到
固体,只能得到![]() ,所以工业上往往用
,所以工业上往往用![]() 和
和![]() 混合后共热来制取无水
混合后共热来制取无水![]() 。
。
①写出蒸干![]() 溶液过程中发生的化学反应方程式__________________________________________________。
溶液过程中发生的化学反应方程式__________________________________________________。
②写出该种制法可行性的原因:_______________________________________________,_______________________________________________________________________。(至少写出两个原因)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用AgNO3溶液分别滴定浓度均为0.01 mol/L的KCl、K2C2O4溶液,所得的沉淀溶解平衡图像如图所示(不考虑C2O42-的水解)。下列叙述正确的是( )
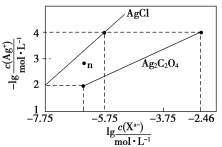
A.Ksp(Ag2C2O4)的数量级等于10-11
B.n点表示AgCl的不饱和溶液
C.向c(Cl-)=c(C2O42-)的混合液中滴入AgNO3溶液时,先生成Ag2C2O4沉淀
D.Ag2C2O4+2Cl-=2AgCl+C2O42-的平衡常数为109.04
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】控制变量是科学研究重要方法。由下列实验现象一定能得出相应结论的是
选项 | A | B | C | D |
装置图 |
|
|
|
|
现象 | 右边试管产生气泡较快 | 左边棉球变棕黄色,右边棉球变蓝色 | B中产生白色沉淀,C中溶液颜色褪去 | 试管中液体变浑浊 |
结论 | 催化活性:Fe3+>Cu2+ | 氧化性:Br2>I2 | 硫酸亚铁铵分解的产物中除NH3外还含有SO3 和SO2 | 非金属性:C>Si |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组设计如图装置,验证黄铜矿(主要成分CuFeS2)在空气中的氧化产物并测定CuFeS2的纯度(杂质不参与反应)。
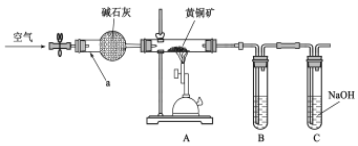
回答下列问题。
(1)仪器a的名称_________,碱石灰的作用______________________________________。
(2)为检验灼烧黄铜矿产生的气体,B中可选__________________
a.HNO3溶液 b.品红溶液 c.BaCl2溶液 d.溴水 e.KMnO4溶液
(3)C中NaOH的作用____________________________________________________
(4)样品经煅烧后的固体中铜元素以泡铜(Cu、Cu2O)形式存在,其中Cu2O能与稀H2SO4反应生成Cu和CuSO4。
①请设计实验验证泡铜中含有Cu2O____________________________________________。
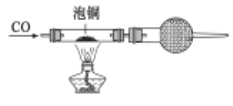
②用泡铜与CO反应来制取粗铜装置如下图,实验时依次进行的操作:
组装仪器→检查装置气密性→加装药品→____________→____________→…→尾气处理;CO还原Cu2O的化学方程式_______________________________________________
(5)为测定CuFeS2的纯度,称取a g黄铜矿样品充分灼烧,从灼烧产物中分离出泡铜,完全溶于稀硝酸,并配成200 mL的溶液,取20.00 mL该溶液用c mol· L-1的标准液EDTA(用H2Y2-表示)滴定至终点(标准液不与杂质反应),消耗EDTA V mL,则CuFeS2的纯度为____________。(滴定时的反应为:Cu2++H2Y2-===CuY2-+2H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com