
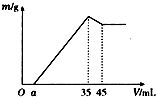
 准确称取6g铝土矿样品(含Al2O3、Fe2O3、SiO2),放入100mL某浓度的HCl溶液中(SiO2不溶于HCl溶液),充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生沉淀的质量m与加入NaOH溶液的体积的关系如图所示,求:
准确称取6g铝土矿样品(含Al2O3、Fe2O3、SiO2),放入100mL某浓度的HCl溶液中(SiO2不溶于HCl溶液),充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生沉淀的质量m与加入NaOH溶液的体积的关系如图所示,求:| 0.35mol |
| 0.1L |
| n |
| c |
| 0.024mol |
| 10mol/L |
| 0.024mol |
| 3 |
| 1 |
| 2 |


科目:高中化学 来源: 题型:
| A、0.21mol?L-1 |
| B、0.42mol?L-1 |
| C、0.56mol?L-1 |
| D、0.26mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol氯气参加氧化还原反应,转移的电子数一定为2NA |
| B、常温常压下,由6 g NO2和40 g N2O4组成的混合气体中原子总数为3NA |
| C、0.1 mol?L-1 NaF溶液中,HF和F-总和为0.1NA个 |
| D、12.5 mL 16 mol?L-1浓硫酸与足量铜反应,生成SO2的分子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、它是由氢气和氧气组成 |
| B、它由两个氢元素和两个氧元素组成 |
| C、每个H2O2分子是由氢元素和氧元素组成 |
| D、每个H2O2分子是由2个氢原子和2个氧原子构成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
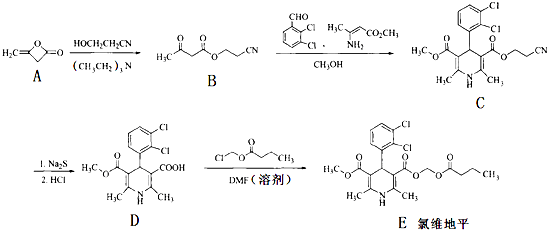
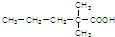 ]是有机合成中间体,请设计合理的方案以丙酮(
]是有机合成中间体,请设计合理的方案以丙酮(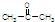 )为唯一有机原料合成2,2-二甲基戊酸(用合成路线流程图表示,并注明反应条件).
)为唯一有机原料合成2,2-二甲基戊酸(用合成路线流程图表示,并注明反应条件).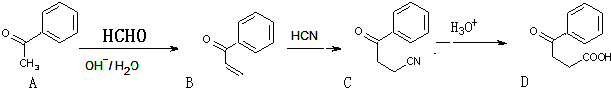
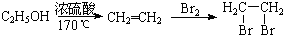
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、8 | B、16 | C、32 | D、48 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Mg2++2HCO3-+2OH-→MgCO3↓+CO32-+2H2O |
| B、Mg2++2HCO3-+2OH-→MgCO3↓+2H2O |
| C、Mg2++2HCO3-+4OH-→Mg(OH)2+2CO32-+2H2O |
| D、HCO3-+OH-→CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
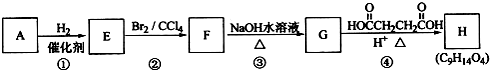
| H+ |
| △ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com