
| A. | 铝热反应是冶炼难熔金属的方法之一 | |
| B. | 铝热剂是混合物 | |
| C. | 活泼金属的冶炼常用电解方法,如电解NaCl溶液就可制备Na | |
| D. | 湿法炼铜的原理是 Fe+CuSO4=Cu+FeSO4 |
分析 金属冶炼一般是用热还原、热分解或电解,铝热反应属于热还原法,铝热剂为铝单质与不活泼金属氧化物的混合物,制备金属钠采用电解熔融的氯化钠,湿法炼铜的原理是 Fe+CuSO4=Cu+FeSO4.
解答 解:A.金属冶炼一般是用热还原、热分解或电解,铝热反应属于热还原法,是冶炼难熔金属的方法之一,故A正确;
B.铝热剂为铝单质与不活泼金属氧化物的混合物,故B正确;
C.制备金属钠采用电解熔融的氯化钠,电解其溶液得不到金属钠,故C错误;
D.湿法炼铜的原理是 Fe+CuSO4=Cu+FeSO4,故D正确.
故选C.
点评 本题考查金属的冶炼,金属的活泼性不同,冶炼方法不同,活泼金属采用电解法冶炼,不活泼的金属采用直接加热法冶炼,大部分金属的冶炼都是在高温下采用氧化还原反应法,题目难度不大.


科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将NaOH浓溶液滴加到饱和FeCl3溶液中制备Fe(OH)3胶体 | |
| B. | 用向上排空气法收集铜粉与稀硝酸反应产生的NO | |
| C. | 配制氯化铁溶液时,将氯化铁溶解在较浓的盐酸中再加水稀释 | |
| D. | 将Cl2与HCl混合气体通过饱和食盐水可得到纯净的Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化性:ClO->I2>SO42- | |
| B. | 蓝色消失的原因是Na2SO3溶液反应生成SO2具有漂白性 | |
| C. | 淀粉KI溶液变蓝是因为I-被ClO-氧化为I2,I2遇淀粉变蓝 | |
| D. | 若将Na2SO3溶液加入溴水,溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
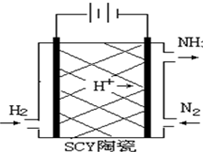 科学家采用质子高导电性的SCY陶瓷(可传递H+)实现了低温常压下高转化率的电化学合成氨,其实验原理示意图如图所示,则阴极的电极反应式是反应式为N2+6H++6e-=2NH3.
科学家采用质子高导电性的SCY陶瓷(可传递H+)实现了低温常压下高转化率的电化学合成氨,其实验原理示意图如图所示,则阴极的电极反应式是反应式为N2+6H++6e-=2NH3.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
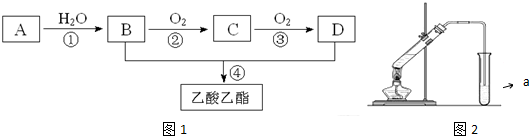
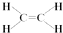 ,C的结构简式:CH3CHO.
,C的结构简式:CH3CHO.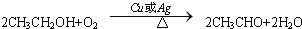 ;反应类型:氧化反应.
;反应类型:氧化反应.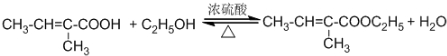 ,为从该实验后的混合气体中分离出乙酸乙酯,右侧试管中所选用的试剂a是饱和碳酸钠溶液,a试剂的作用是中和乙酸、吸收乙醇、降低乙酸乙酯在溶液中的溶解度,有利于分层析出.
,为从该实验后的混合气体中分离出乙酸乙酯,右侧试管中所选用的试剂a是饱和碳酸钠溶液,a试剂的作用是中和乙酸、吸收乙醇、降低乙酸乙酯在溶液中的溶解度,有利于分层析出.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com